心脏骤停(cardiac arrest, CA)作为最危重的急症,存活率很低, 其中院内CA 6%~26%,院外CA通常 < 10%[1-2]。近年来,体外心肺复苏(extracorporeal cardiopulmonary resuscitation, ECPR)正越来越多地应用于救治CA患者。ECPR是一种在传统CPR过程中利用体外膜肺氧合(extracorporeal membrane oxygenation, ECMO)技术改善血流动力学,增加重要脏器灌注,为逆转CA病因赢得时间的方法[3]。然而目前缺乏经过验证的评分系统来预测这一人群的死亡风险。静脉-动脉ECMO后生存(survival after veno-arterial ECMO, SAVE)评分最初是Schmidt等[4]为顽固性心源性休克接受ECMO治疗的患者而创建的,但他们的研究中排除了ECPR患者,且该评分系统不包含血乳酸值这一参数。乳酸被认为是组织灌注的标志。越来越多的证据表明,ECMO支持期间乳酸水平对病死率有预测作用[5-6]。本文通过回顾性研究探讨SAVE评分联合上机24 h乳酸对ECPR患者预后的预测价值。
1 资料与方法 1.1 一般资料回顾2017年4月至2021年6月间因CA于南京医科大学第一附属医院急诊科行ECPR治疗的患者共79例。排除临床资料不全(7例)及VA-ECMO转机时间小于24 h(13例)的病例,最终共59例患者被纳入研究。根据28 d生存情况,分为生存组与死亡组。收集患者的一般信息、合并症、ECMO上机诊断、ECMO上机前实验室指标、上机后24 h血乳酸水平、治疗情况及其他数据等,并计算SAVE评分。本研究伦理审批号为2020-SR-226, 已获得患者知情同意。
1.2 ECMO的建立本中心备有急诊ECMO专用成套设备,使用的是德国迈柯唯公司生产的离心泵、氧合器、肝素涂层穿刺包及动静脉导管。所有患者ECMO的建立途径均为床旁经皮经股动静脉穿刺置管,股动脉灌注管一般选择15-17 Fr,股静脉引流管根据置管医师经验通常采用19-21 Fr。具体详见本中心前期经验[7]。
1.3 统计学方法应用SPSS 25.0统计软件进行数据分析,通过Shaprio-Wilk检验连续数值资料正态性。正态分布的计量资料采用均数±标准差(x±s)表示,两组间比较采用独立样本t检验。偏态分布的计量资料以中位数和四分位数[M(Q1,Q3)]表示,两组间比较采用非参数Mann-Whitney U检验。计数资料以例(%)表示,组间比较采用χ2或Fisher确切概率法检验。通过二元logistic回归分析ECPR患者28 d死亡相关影响因素;绘制受试者工作特征(ROC)曲线评估影响因素预测价值,并计算ROC曲线下面积(AUC), 确定截断值,计算敏感度、特异度。以P < 0.05为差异有统计学意义。
2 结果 2.1 比较存活组和死亡组间基线资料本研究共纳入ECPR患者59例,其中死亡组36例,存活组23例,存活率为39%。两组患者在年龄、既往史[包括高血压、糖尿病、冠心病、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)、脑梗塞]、吸烟饮酒史、急性生理学慢性健康(acute physiology and chronic health evaluation, APACHE)Ⅱ评分、初始乳酸、上机前实验室指标(包括白细胞计数、中性粒细胞计数、血红蛋白、血小板、红细胞分布宽度、丙氨酸转氨酶、谷草转氨酶、血尿素氮、肌酐、血钾、血钠、血氯、血钙浓度、降钙素原)、CA时间、主动脉内球囊反搏(intra-aortic balloon pump, IABP)的差异无统计学意义(P >0.05)。
两组患者在性别(P=0.040)、SAVE评分(P < 0.001)、上机24 h乳酸(P < 0.001)、CA至CPR时间(P=0.016)、连续性肾脏替代治疗(continuous renal replacement therapy, CRRT)(P=0.011)上差异有统计学意义。死亡组SAVE评分明显低于存活组,而上机后24 h血乳酸明显高于存活组。见表 1。
| 指标 | 存活组(n=23) | 死亡组(n=36) | P值 |
| 年龄(岁)a | 47.83±16.49 | 45.06±18.06 | 0.555 |
| 性别 | 0.040 | ||
| 男(例) | 12(52.2) | 28(77.8) | |
| 女(例) | 11(47.8) | 8(22.2) | |
| SAVE评分(分)a | -2.43±4.77 | -11.67±4.60 | < 0.001 |
| APACHE Ⅱ评分(分)b | 36(33, 37) | 36.5(33, 38.75) | 0.248 |
| 上机24 h乳酸(mmol/L)b | 1.65(1.07, 3.15) | 5.94(3.37, 12.40) | < 0.001 |
| 既往史、个人史(例,%) | |||
| 高血压 | 5(21.7) | 12(33.3) | 0.338 |
| 糖尿病 | 3(13.0) | 5(13.9) | 0.926 |
| 冠心病 | 4(17.4) | 4(11.1) | 0.492 |
| COPD | 0(0) | 0(0) | 1.000 |
| 脑梗塞 | 0(0) | 3(8.3) | 0.155 |
| 吸烟 | 3(13.0) | 12(33.3) | 0.081 |
| 饮酒 | 2(8.7) | 1(2.8) | 0.313 |
| ECMO上机诊断(例,%) | 0.051 | ||
| 心肌炎 | 6(26.1) | 2(5.6) | |
| 心肌梗死 | 7(30.4) | 19(52.8) | |
| 其他 | 10(43.5) | 15(41.7) | |
| ECMO前实验室指标 | |||
| 初始乳酸(mmol/L)b | 7.51(4.17, 15.00) | 11.43(6.40, 17.91) | 0.082 |
| 白细胞(×109/L)b | 18.12(10.73, 23.70) | 14.87(10.96, 20.00) | 0.393 |
| 中性粒细胞(×109/L)b | 13.76(8.11, 21.29) | 9.68(5.55, 17.26) | 0.142 |
| 血红蛋白(g/L)b | 123.0(106, 136) | 133.5(123.50, 147.75) | 0.061 |
| 红细胞分布宽度(%)b | 12.8(12.4, 13.4) | 12.9(12.15, 13.45) | 0.901 |
| 血小板(×109/L)b | 183(151, 232) | 182(127, 242.5) | 0.641 |
| 丙氨酸转氨酶(U/L)b | 134.0(68.3, 270.2) | 320.0(127.65, 622.25) | 0.060 |
| 谷草转氨酶(U/L)b | 269.7(92.3, 683.1) | 759.3(116.05, 1283.85) | 0.231 |
| 血尿素氮(mmol/L)b | 7.36(5.54, 9.7) | 6.61(5.06, 9.86) | 0.263 |
| 肌酐(umol/L)b | 102.7(81.4, 123.8) | 118.1(95.23, 138.98) | 0.140 |
| K+(mmol/L)a | 3.79±0.61 | 4.00±1.01 | 0.379 |
| Na+(mmol/L)a | 141.81±5.30 | 142.86±5.93 | 0.491 |
| Ca2+(mmol/L)a | 2.01±0.20 | 1.97±0.27 | 0.602 |
| Cl-(mmol/L)a | 105.43±4.97 | 103.56±5.03 | 0.168 |
| 降钙素原(ng/mL)b | 1.81(0.29, 5.72) | 1.42(0.10, 7.34) | 0.793 |
| 心脏骤停至CPR时间(min)b | 0(0, 0) | 1(0, 11.5) | 0.016 |
| 心脏骤停时间(in)b | 40(20, 65) | 50.5(27.5, 80.25) | 0.355 |
| 治疗 | |||
| CRRT(例) | 15 | 33 | 0.011 |
| IABP(例) | 4 | 13 | 0.122 |
| 注:a为x±s,b为M(Q1,Q3);COPD为慢性阻塞性肺疾病;CRRT为连续性肾脏替代治疗;IABP为主动脉内球囊反搏 | |||
以ECPR患者28 d生存情况为因变量,将上述单因素差异存在统计学差异的变量纳入多因素Logistic回归分析,并构建最佳预测模型,该模型正确预测率86.4%。SAVE评分是体外心肺复苏患者死亡的保护因素(OR=0.703,95%CI:0.566~0.873,P=0.001);上机24 h乳酸是体外心肺复苏患者死亡的危险因素(OR=1.608,95%CI:1.025~2.523,P=0.039)。详见表 2、图 1。
| 变量 | logistic回归分析 | ROC | |||||||
| B | OR值 | 95%CI | P值 | AUC | 最佳截断值 | 敏感度(%) | 特异度(%) | ||
| SAVE评分 | −0.352 | 0.703 | 0.566~0.873 | 0.001 | 0.917 | −6.0 | 78.30 | 91.70 | |
| 上机24 h乳酸 | 0.475 | 1.608 | 1.025~2.523 | 0.039 | 0.847 | 4.7 | 63.90 | 100.00 | |
| SAVE评分+上机24 h乳酸 | 0.952 | — | 82.60 | 100.00 | |||||

|
| 图 1 ECPR患者SAVE评分及上机24 h乳酸对28 d死亡的预测概率 Fig 1 Prediction probability of 28-day mortality of SAVE score and 24-h lactate in patients with ECPR |
|
|
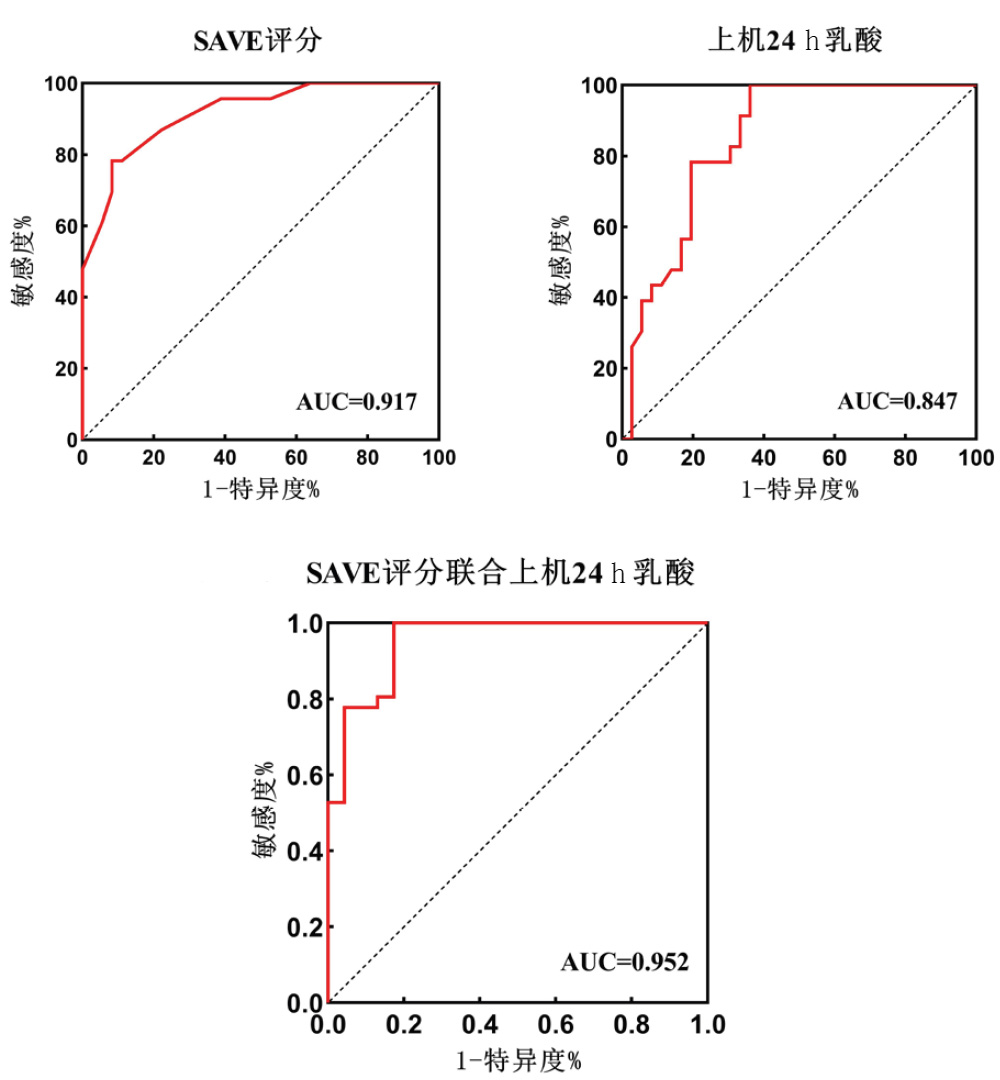
采用ROC曲线对SAVE评分、24 h血乳酸值进行分析,SAVE评分预测ECPR患者28 d死亡风险的AUC是0.917,最佳截断值为-6分(敏感度78.30%,特异度91.70%)。24 h乳酸的AUC是0.847,最佳截断值为4.7 mmol/L(敏感度63.90%,特异度100.00%)。SAVE评分和上机24 h乳酸联合预测时,其AUC为0.952,大于两者单独预测的AUC。见表 2、图 2。
|
| 图 2 ECPR患者SAVE评分、上机24 h乳酸及两者联合预测预后的ROC曲线 Fig 2 ROC curve for predicting prognosis of SAVE score, 24-h lactate and their combination in patients with ECPR |
|
|
2015年Schmidt等[4]通过一项大规模回顾性研究创建了SAVE评分,该评分目前已被ELSO[8]推荐用于预测VA-ECMO患者的预后,内容主要包括诊断、年龄、循环参数、通气参数、继发性器官功能障碍(例如肾功能、肝功能、神经功能)和先前存在的合并症等变量。CA史是这一评分中的一个重要变量,然而,插管期间持续心脏停搏即ECPR患者,考虑到其高病死率而被该研究排除。CA患者接受ECPR治疗出院生存率为17.6%~50.0%,结果各不相同[9-12]。ELSO组织截止2021年更新的数据显示成人ECPR总体生存率29%[13]。目前还没有经过验证的评分系统来预测ECPR患者的预后。故本研究检测了SAVE评分预测ECPR患者预后的有效性,结果显示生存组SAVE评分明显高于死亡组(P < 0.001),ROC曲线下面积达0.917,预测能力与Schmidt等[4]在“外部”队列中的验证相当。本队列较高的存活率,即与死亡相关的中低评分比例较小可能解释这一较高的ROC曲线下面积。本研究纳入的59例ECPR患者平均SAVE值-6, 参照Schmidt等[4]的研究,存活率为30%,而本项研究入组患者存活率为39%,高于30%。有几点可以解释:一是本院急诊具备体外循环团队,可在CA第一时间开展ECPR治疗,节省了会诊、仪器搬运等时间,因此ECPR成功率略高;其次SAVE评分排除ECMO插管之后的实验室数据可能会忽略这些患者病情的动态变化从而低估了存活率;另外本研究排除了ECMO运转不足24 h的患者,这部分患者上机后24 h内死亡。
乳酸是组织灌注的一个指标,因此可以作为心肺复苏质量的替代指标。通过动脉血气分析很容易可以得到一组结果。一些研究表明,在因心脏和非心脏原因接受ECLS治疗的患者中,高乳酸血症与死亡率密切相关[14-15]。Chen等[16]提出将ECLS开始前的乳酸水平合并到SAVE评分中,但初始乳酸水平可能有其自身的局限性。因为ECMO通常可以提供完全氧合循环支持,从而满足严重呼吸或循环衰竭患者的氧气输送和全身组织灌注,因此,这些患者的乳酸水平有望迅速下降;此外还要考虑到一些血管活性药物对乳酸水平的影响及乳酸自身变化的延迟性等[17]。Park等[18]的研究显示ECMO上机后前24 h血清乳酸峰值可预测急性心肌梗死合并CS和CA患者30 d的病死率。Lin等[19]将ECMO插管后16 h的乳酸纳入SAVE评分,提高了ECMO患者病死率的预测价值。本研究中存活者与死亡者初始乳酸水平差异无统计学意义, 但存活组24 h乳酸水平明显低于死亡组(P < 0.001),且24 h乳酸水平在区分病死率方面的敏感性和特异性较好(AUC=0.847,95%CI: 1.025~2.523;P=0.039)。因此笔者认为上机后24 h乳酸能更好的反映所用血管活性药物药物、平均动脉压变化以及肝脏和其他重要器官对大循环的影响。
本研究通过绘制ROC曲线发现SAVE评分对和24 h血乳酸水平预测ECPR患者28 d死亡风险的AUC分别为0.917、0.847, SAVE评分对ECPR患者预后的预测效能稍高于24 h血乳酸,两者联合病死率预测的AUC最高,为0.952,效能明显高于两个指标单独预测。因此,SAVE评分对ECPR患者预后具有一定预测能力, 与24 h血乳酸水平联合检测有助于提高预测的准确性。
综上所述, SAVE评分降低和24 h血乳酸升高是ECPR患者28 d死亡的危险因素,可能提示ECPR患者病情较重及预后不良,两者联合检测对评估ECPR患者预后具有较高的指导意义。但本研究为单中心研究, 纳入的病例数有限, 剔除了部分不符合研究标准患者, 故需要更大样本的研究来验证。此外,血乳酸清除率及乳酸动态监测的研究不断发展,本研究未动态监测乳酸变化,对于其在ECPR患者预后预测中的价值需进一步研究证实。
利益冲突 所有作者声明无利益冲突
作者贡献声明 邹乐:研究设计、采集数据、统计学分析、论文撰写;朱轶、张忠满:研究设计、统计学分析;安迪、夏雨、丁涛、时育彤:采集数据;梅勇、吕金如、李伟、陈旭锋:论文修改、指导支持
| [1] | Wong CX, Brown A, Lau DH, et al. Epidemiology of sudden cardiac death: global and regional perspectives[J]. Heart Lung Circ, 2019, 28(1): 6-14. DOI:10.1016/j.hlc.2018.08.026 |
| [2] | Abrams D, MacLaren G, Lorusso R, et al. Extracorporeal cardiopulmonary resuscitation in adults: evidence and implications[J]. Intensive Care Med, 2022, 48(1): 1-15. DOI:10.1007/s00134-021-06514-y |
| [3] | Panchal AR, Berg KM, Hirsch KG, et al. 2019 American heart association focused update on advanced cardiovascular life support: use of advanced airways, vasopressors, and extracorporeal cardiopulmonary resuscitation during cardiac arrest: an update to the American heart association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care[J]. Circulation, 2019, 140(24): e881-e894. DOI:10.1161/CIR.0000000000000732 |
| [4] | Schmidt M, Burrell A, Roberts L, et al. Predicting survival after ECMO for refractory cardiogenic shock: the survival after veno-arterial-ECMO (SAVE)-score[J]. Eur Heart J, 2015, 36(33): 2246-2256. DOI:10.1093/eurheartj/ehv194 |
| [5] | Li CL, Wang H, Jia M, et al. The early dynamic behavior of lactate is linked to mortality in postcardiotomy patients with extracorporeal membrane oxygenation support: a retrospective observational study[J]. J Thorac Cardiovasc Surg, 2015, 149(5): 1445-1450. DOI:10.1016/j.jtcvs.2014.11.052 |
| [6] | Rigamonti F, Montecucco F, Boroli F, et al. The peak of blood lactate during the first 24h predicts mortality in acute coronary syndrome patients under extracorporeal membrane oxygenation[J]. Int J Cardiol, 2016, 221: 741-745. DOI:10.1016/j.ijcard.2016.07.065 |
| [7] | 梅勇, 陈旭锋, 张劲松, 等. 急诊医护团队主导体外膜肺氧合应用的经验探讨[J]. 中华急诊医学杂志, 2017, 26(10): 1115-1119. DOI:10.3760/cma.j.issn.1671-0282.2017.10.003 |
| [8] | Extracorporeal Life Support Organization. ELSO Guidelines for Patient Care, Respiratory & Cardiac Support, ECMO in COVID-19[EB/OL]. (2021-06-15)[2022-03-09]. https://www.elso.org/resources/guidelines.aspx. |
| [9] | Twohig CJ, Singer B, Grier G, et al. A systematic literature review and meta-analysis of the effectiveness of extracorporeal-CPR versus conventional-CPR for adult patients in cardiac arrest[J]. J Intensive Care Soc, 2019, 20(4): 347-357. DOI:10.1177/1751143719832162 |
| [10] | Blumenstein J, Leick J, Liebetrau C, et al. Extracorporeal life support in cardiovascular patients with observed refractory in-hospital cardiac arrest is associated with favourable short and long-term outcomes: a propensity-matched analysis[J]. Eur Heart J Acute Cardiovasc Care, 2016, 5(7): 13-22. DOI:10.1177/2048872615612454 |
| [11] | Choi DS, Kim T, Ro YS, et al. Extracorporeal life support and survival after out-of-hospital cardiac arrest in a nationwide registry: a propensity score-matched analysis[J]. Resuscitation, 2016, 99: 26-32. DOI:10.1016/j.resuscitation.2015.11.013 |
| [12] | Dennis M, McCanny P, D'Souza M, et al. Extracorporeal cardiopulmonary resuscitation for refractory cardiac arrest: a multicentre experience[J]. Int J Cardiol, 2017, 231: 131-136. DOI:10.1016/j.ijcard.2016.12.003 |
| [13] | Guerguerian AM, Sano M, Todd M, et al. Pediatric extracorporeal cardiopulmonary resuscitation ELSO guidelines[J]. ASAIO J, 2021, 67(3): 229-237. DOI:10.1097/MAT.0000000000001345 |
| [14] | Jung C, Janssen K, Kaluza M, et al. Outcome predictors in cardiopulmonary resuscitation facilitated by extracorporeal membrane oxygenation[J]. Clin Res Cardiol, 2016, 105(3): 196-205. DOI:10.1007/s00392-015-0906-4 |
| [15] | Laimoud M, Alanazi M. The clinical significance of blood lactate levels in evaluation of adult patients with veno-arterial extracorporeal membrane oxygenation[J]. Egypt Heart J, 2020, 72(1): 74. DOI:10.1186/s43044-020-00108-7 |
| [16] | Chen WC, Huang KY, Yao CW, et al. The modified SAVE score: predicting survival using urgent veno-arterial extracorporeal membrane oxygenation within 24 hours of arrival at the emergency department[J]. Crit Care, 2016, 20(1): 336. DOI:10.1186/s13054-016-1520-1 |
| [17] | Levy B, Perez P, Perny J, et al. Comparison of norepinephrine-dobutamine to epinephrine for hemodynamics, lactate metabolism, and organ function variables in cardiogenic shock. A prospective, randomized pilot study[J]. Crit Care Med, 2011, 39(3): 450-455. DOI:10.1097/CCM.0b013e3181ffe0eb |
| [18] | Park SJ, Kim SP, Kim JB, et al. Blood lactate level during extracorporeal life support as a surrogate marker for survival[J]. J Thorac Cardiovasc Surg, 2014, 148(2): 714-720. DOI:10.1016/j.jtcvs.2014.02.078 |
| [19] | Lin TT, Lin MH, Wu CK, et al. Early lactate changes improve the outcome prediction for extracorporeal membrane oxygenation[J]. Eur J Cardiothorac Surg, 2020, 58(5): 915-922. DOI:10.1093/ejcts/ezaa171 |
 2022, Vol. 31
2022, Vol. 31




