2 内蒙古医科大学附属医院急诊科,呼和浩特 010059
2 Emergency Department, the Affiliated Hospital of Inner Mongolia Medical University, Huhhot 010059, China
心脏骤停后综合征(post-cardiac arrest syndrome,PCAS)是心肺复苏后机体发生的一系列复杂的病理生理改变,包括心脏骤停后脑损伤、心肌功能障碍、全身性缺血-再灌注损伤和持续诱发性病变[1]。发生PCAS实际上就是机体发生全身器官再灌注的结果,即缺血-再灌注后出现组织损伤加重或不可逆损伤,称为缺血-再灌注损伤(ischemia reperfusion injury, IRI)。全身炎症反应综合征(systemic inflammatory response syndrome, SIRS)、氧化应激反应在IRI的发生中起重要作用[2]。代表性炎因子有肿瘤坏死因子-α(tumor necrosis factor -α, TNF-α)、白细胞介素-6(interleukin-6, IL-6),TNF-α在炎症反应中有启动、触发的作用,诱发其他炎症介质。炎症因子与缺血-再灌注后细胞的实质损伤密切相关,可以反映机体炎症反应的严重性[3]。超氧化物歧化酶(superoxide dismutase, SOD)、丙二醛(malondialdehyde, MDA)是氧化应激反应中重要的氧自由基,SOD活力的高低代表了机体清除氧自由基的能力。MDA可以反应细胞氧化应激损伤的程度。缺血修饰蛋白(ischemia modified albumin, IMA)是反应心肌缺血的敏感指标[4]。乌司他丁(ulinastatin, UTI)是一种广谱的蛋白酶抑制剂,具有抑制水解酶,稳定溶酶体膜,抑制多种炎症介质及免疫调节作用[5-7],减轻缺血-再灌注造成的脑组织损伤[8]。本研究中通过猪心脏骤停(cardiac arrest, CA)模型评价复苏时应用UTI对防治PCAS的效果。
1 材料与方法 1.1 实验动物3~4个月龄雄性北京长白猪12只,体质量(30±2) kg,购自北京注册实验动物中心,许可证号SCXK 11-00-002。本研究动物实验实施过程符合实验动物伦理要求。
1.2 方法 1.2.1 分组12只造模后存活11只,随机数字法分为UTI组6只、对照组5只;对照组开始进行CPR同时缓慢静推5 mL生理盐水;UTI组开始进行CPR同时缓慢静推UTI 100 000 U(溶于生理盐水5 mL)。每3 h注射1次,直至复苏后24 h(第24 h不给药)。
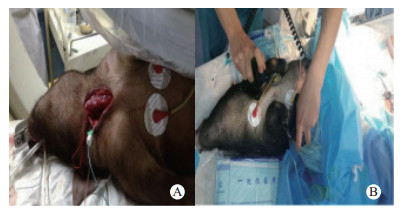
1.2.2 模型建立按照文献[9], 实验猪术前禁食12 h、禁水2 h。戊巴比妥钠30 mg/kg经耳缘静脉实施静脉全麻,此后戊巴比妥钠8 mg/(kg·h)维持麻醉状态。麻醉完毕后,经口行气管插管,连接呼吸机(吸入氧体积分数21%, 通气频率12次/min,潮气量15 mL/kg)。连接心电监护,手术暴露右颈内静脉或右侧股静脉留置6 F鞘管,放置刺激电极,插入约20~25 cm可进入右心室,用于诱发室颤和抽取静脉血。采用穿刺右侧股动脉留置动脉导管监测动脉压(图 1A)。
|
| A:实验猪制作CA模型前准备;B:实验猪电除颤 图 1 实验动物模型制备和电除颤 Fig 1 Preparation of experimental pigs and electric defibrillation |
|
|
应用S1S2程控刺激法诱发猪室颤以制作心脏骤停模型:将心室内电极导线连接程控刺激仪,选择食道输出电压40 V,S1S2(300/200 ms)模式,8:1,步长-10 ms连续程控刺激,直到出现室颤。室颤成功后,断开呼吸机,停止机械通气。室颤5 min后开始CPR,同时给药。先给予标准胸外按压2 min,按压通气比30:2,行2~3个周期的CPR;如未成功,开始电除颤,能量选择为150 J(双向指数截断波)除颤至复律,A电极板位于猪心尖部,S电极板位于心底部(间隔距离大于5 cm)(图 1B)。自主循环恢复的标准是:室上性自主心律伴平均动脉压大于50 mmHg(1 mmHg=0.133 kPa),持续5 min以上。
1.2.4 检测指标分别于室颤前、室颤后2、4、6、12、18、24 h抽取动物静脉血,采用酶联免疫吸附试验(ELISA)测定TNF-α、IL-6、SOD、MDA,IMA另ROSC后1 h的取血检测。
1.2.5 病理取材及光镜标本处理两组动物均于复苏后24 h再次麻醉后处死,迅速取左心室心尖。固定24 h,脱水、透明、包埋、切片、HE染色。各组随机挑选3张切片显微镜下观察缺血区病理形态学改变。
1.3 统计学方法数据处理采用SPSS 17.0统计软件,计量资料用均数±标准差(Mean±SD)表示,组间比较采用LSD-t检验和重复测量的方差分析。以P < 0.05为差异有统计学意义。
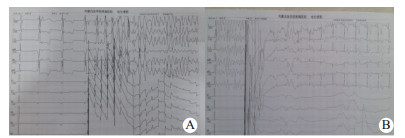
2 结果 2.1 室颤心电图实验猪诱颤成功时心室波均呈连续大幅度波形,大小不等,形态不同(图 2A)、两组实验猪CPR成功后心电图恢复自主心律(图 2B)。
|
| 图 2 室颤心电图(A)和除颤后心电图(B) Fig 2 Ventricular electrocardiogram and electrocardiogram after ventricular fibrillation |
|
|
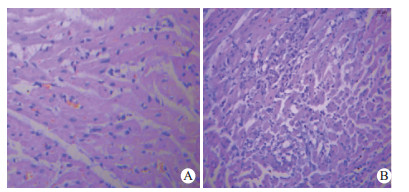
HE染色后光镜下观察显示,UTI组心肌纤维排列尚整齐,肌纤维肿胀,可见少量断裂,细胞核形态,大小不均匀,心肌间质可见少量炎症细胞浸润(图 3A)。对照组心肌纤维肿胀断裂、扭曲,呈波浪状,排列极度紊乱,伴有横纹消失,并可见大片心肌纤维溶解坏死,心肌间质可见大量炎症细胞浸润,间隙增宽,心肌细胞出现空泡变性及溶解,心肌细胞形态欠规则,大小不均(图 3B)。
|
| A: UTI组心肌组织病理学改变;B:对照组心肌组织病理学改变 图 3 UTI组和对照组心肌组织病理学改变(HE×200) Fig 3 Myocardiac histopathological changes in the UTI and control groups (HE×200) |
|
|
室颤前,两组猪血清TNF-α、IL-6水平差异无统计学意义(P > 0.05)。室颤后,UTI组2 h时TNF-α、IL-6水平明显低于对照组,差异有统计学意义(P < 0.05),见表 1。
| 组别 | 时间 | TNF-α | t值 | P值 | IL-6 | t值 | P值 |
| UTI组 | 室颤前 | 18.96±3.49 | -1.623 | 0.139 | 19.92±3.84 | -0.049 | 0.962 |
| (n=6) | ROSC 2 h | 22.11±2.37a | 5.147 | 0.001 | 25.62±0.69a | 5.445 | < 0.01 |
| ROSC 4 h | 28.52±2.22a | 4.100 | 0.003 | 29.22±2.32a | 6.311 | < 0.01 | |
| ROSC 6 h | 35.01±2.92a | 4.456 | 0.002 | 29.22±2.30a | 6.500 | < 0.01 | |
| ROSC 12 h | 63.73±9.73a | 3.572 | 0.006 | 40.23±0.38a | 6.968 | < 0.01 | |
| ROSC 24 h | 78.97±5.47a | 3.764 | 0.005 | 51.47±1.14a | 6.763 | < 0.01 | |
| 对照组 | 室颤前 | 21.79±1.83 | 19.84±1.04 | ||||
| (n=5) | ROSC 2 h | 28.15±1.19 | 27.78±0.62 | ||||
| ROSC 4 h | 33.53±1.74 | 44.98±7.10 | |||||
| ROSC 6 h | 42.15±2.26 | 46.58±3.20 | |||||
| ROSC 12 h | 80.38±3.88 | 54.20±3.58 | |||||
| ROSC 24 h | 102.35±7.69 | 68.35±4.26 | |||||
| 注:UTI,乌司他丁;TNF-α,肿坏死因子-α;IL-6,白细胞介素-6;与对照组同时点比较,aP < 0.05 | |||||||
室颤前,两组猪血清MDA、SOD水平差异无统计学意义(P > 0.05)。室颤后,UTI组4 h起MDA水平明显低于对照组,差异有统计学意义(P < 0.05)。UTI组4 h起SOD水平明显高于对照组,差异有统计学意义(P < 0.05),见表 2。
| 组别 | 时间 | SOD) | t值 | P值 | MDA | t值 | P值 |
| UTI组 | 室颤前 | 69.41±7.13 | -0.394 | 0.703 | 4.18±0.38 | -0.413 | 0.689 |
| (n=6) | ROSC 2 h | 67.99±6.36 | -1.720 | 0.120 | 4.91±0.34 | 0.733 | 0.482 |
| ROSC 4 h | 61.13±4.95 a | -3.835 | 0.004 | 5.82±0.42a | 5.667 | < 0.01 | |
| ROSC 6 h | 51.65±2.58 a | -4.246 | 0.002 | 6.75±0.72a | 5.342 | < 0.01 | |
| ROSC 12 h | 35.70±2.89 a | -6.200 | 0.000 | 9.50±0.68a | 5.873 | < 0.01 | |
| ROSC 24 h | 24.74±1.70 a | -4.238 | 0.002 | 11.87±1.02a | 5.886 | < 0.01 | |
| 对照组 | 室颤前 | 67.36±10.18 | 4.06±0.53 | ||||
| (n=5) | ROSC 2 h | 61.97±4.95 | 5.06±0.37 | ||||
| ROSC 4 h | 51.45±2.92 | 7.34±0.48 | |||||
| ROSC 6 h | 43.06±4.10 | 10.11±1.33 | |||||
| ROSC 12 h | 22.44±4.19 | 12.71±1.12 | |||||
| ROSC 24 h | 16.63±2.61 | 15.23±1.27 | |||||
| 注:UTI,乌司他丁;SOD,超氧化物歧化酶;MDA,丙二醛;与对照组同时点比较,aP < 0.05 | |||||||
室颤前,两组猪血清IMA水平差异无统计学意义(P > 0.05)。室颤后1 h时明显升高,UTI组1 h时水平明显低于对照组,差异有统计学意义(P < 0.05),但12 h时两组比较,差异无统计学意义(P > 0.05),见表 3。
| 组别 | 时间 | IMA | t值 | P值 |
| UTI组 | 室颤前 | 2.28±0.17 | -1.024 | 0.333 |
| (n=6) | ROSC1 h | 5.85±0.21a | 3.393 | 0.008 |
| ROSC2 h | 7.16±0.87a | 2.912 | 0.017 | |
| ROSC4 h | 9.6±0.50a | 4.874 | 0.001 | |
| ROSC6 h | 10.87±0.59a | 3.859 | 0.004 | |
| ROSC12 h | 5.24±1.06 | 0.941 | 0.371 | |
| ROSC 24 h | 3.37±0.27 | -1.296 | 0.227 | |
| 对照组 | 室颤前 | 2.15±0.25 | ||
| (n=5) | ROSC1 h | 6.46±0.38 | ||
| ROSC2 h | 8.87±0.47 | |||
| ROSC4 h | 11.00±0.44 | |||
| ROSC6 h | 11.76±0.12 | |||
| ROSC12 h | 5.71±0.36 | |||
| ROSC 24 h | 3.45±0.67 | |||
| 注:UTI,乌司他丁;IMA,缺血修饰白蛋白;与对照组同时点比较,aP < 0.05 | ||||
多脏器功能衰竭的发生发展与缺血-再灌注损伤的时间成正相关,ROSC时间越长,身体各器官组织细胞发生缺血、缺氧时间越长,细胞损伤越严重,脏器衰竭程度越严重,越容易发生MODS。研究发现,ROSC发生在5 min内,机体缺血缺氧时间较短,脏器受损程度相对较轻,治疗结果较好;ROSC超过10 min后,组织细胞将遭受不可逆损伤,脏器受损程度及受累数目较前者明显加重,更容易发生MODS,导致死亡风险的增加。所以尽量将ROSC时间降至最低,是急危重症患者抢救过程中的重中之重。所以本文所涉及实验模型复苏时间均在室颤诱导成功后5 min。
UTI是一种胰蛋白酶抑制剂,具有很强的胰蛋白酶抑制作用,已有较多实验及研究发现UTI和它的分解代谢产物可以通过其高效的抑酶能力,抑制多种水解酶的活性及其释放量,影响甚至抑制了水解酶参与的全身炎症反应,并改善组织器官灌注[10];此外,UTI可以通过抑制内皮细胞黏附分子表达,来改善毛细血管通透性,充分改善毛细血管通透性增加等情况导致的微循环淤堵情况;同时在维持内源性血管活性物质平衡、改善组织灌注方面也有作用,因为前列腺素H2合酶2表达被其有效抑制,从而血栓素B2浓度明显下降;且UTI分子中第10位的丝氨酸上的硫酸软骨素糖链带有负电荷,它与细胞膜受体结合后直接阻断缺血-再灌注损伤发生时因钙超载引起的磷脂酶激活途径,进一步减少溶酶体膜等生物膜的损害,维持生物膜生理功能,同时清除氧自由基,减少并抑制心肌抑制因子生成,从而达到稳定细胞膜、减少脏器缺血的目的,进而有效减轻缺血-再灌注对脏器的损伤,控制全身炎症反应的发生[11-13]。
光镜下,ROSC后通过HE染色后可见心肌组织出现明显缺血改变。室颤后脑组织内出现持续的缺血缺氧,在约4 min后脑内储存的能量即消耗殆尽,此时细胞外Na+内流,触发Na+- Ca2+交换体,增加Ca2+内流,细胞内钙超载又激活蛋白酶,直接破坏生物膜的完整性,进一步扩大炎症、氧化应激反应[14]。UTI组药物干预后较对照组心肌组织病理损伤有明显减轻,UTI可明显稳定细胞膜, 减少ROSC后早期能量消耗、减轻钙超载、减少氧自由基释放等级联效应有关。
炎症因子在心肺复苏后IRI的释放对心肌功能有抑制作用[15]。缺血缺氧性损伤后机体的应激反应、炎症反应系统在ROSC早期启动,随着致炎因子增多,损伤逐渐扩大,IL-6刺激机体发生炎症反应的同时引起血管活性物质产生,并通过链式扩大效应造成广泛组织损伤。TNF-α也是炎症反应中的关键性介质,当机体发生缺血缺氧性损伤并发炎症反应或免疫反应时,细胞的携氧能力降低,TNF-α反应性增高,可增强中性粒细胞对血管内皮的黏附性,甚至产生菌溶刺激因子,缓解组织缺氧情况。其高表达可部分拮抗缺血-再灌注损伤所产生的应激反应,减少对机体的冲击。本实验中ROSC后2~24 h,两组血清IL-6、TNF-α水平均明显升高,说明各器官组织缺血-再灌注损伤重,而UTI组在各时间点均优于对照组,说明UTI给药对组织器官的炎症反应具有保护作用。
SOD在体内发挥重要的抗氧化作用,严重缺血缺氧损伤会破坏细胞屏障功能,SOD仅在此时可进入血液[16]。本实验结果显示,ROSC后4 h时,血清SOD水平均明显升高,说明缺血-再灌注损伤极严重,而UTI组在各时间点均优于对照组,说明UTI给药对细胞屏障系统具有保护作用,提高组织抗氧化应激等能力。
MDA可以反映细胞氧化应激损伤的程度。在生物体内,自由基作用于脂质发生过氧化反应,氧化终产物为MDA,会引起蛋白质、核酸等生命大分子的交联聚合,且具有细胞毒性。脂质氧化终产物MDA在体外影响线粒体呼吸链复合物及线粒体内关键酶活性。它是膜脂过氧化最重要的产物之一,它的产生还能加剧细胞膜损伤,因此可通过MDA了解膜脂过氧化的程度[17]。本实验结果显示,ROSC后4 h时,血清MDA水平均明显降低,说明缺血-再灌注损伤造成严重细胞膜过氧化,而UTI组在各时间点均优于对照组,说明UTI后处理IRI猪体内脂质过氧化反应减弱,而抗氧化应激的能力得以增强。
IMA是人血清白蛋白在通过缺血器官时产生的,可敏感地反映心肌缺血状况,在缺血-再灌注发生时,由于自由基等破坏了血清白蛋白的氨基酸序列,而导致白蛋白与过渡金属的结合能力改变,这种因缺血而发生与过渡金属结合能力改变的白蛋白则称缺血修饰白蛋白。ROSC后组织细胞缺血、缺氧造成的能量代谢障碍,兴奋性神经介质释放,钙离子过量的内流,自由基反应造成细胞死亡等缺血性的连锁的反应,生成大量的缺血修饰白蛋白[4]。本实验结果表明,复苏后1 h开始IMA较实验前明显升高,说明ROSC后心肌很快开始出现心肌缺血。复苏后2、4、6 h IMA持续升高,但12 h时两组比较差异无统计学意义。UTI组IMA升高水平明显低于对照组,说明IMA心脏骤停后快速升高(1 h),持续12 h,UTI具有减轻心肺复苏后心肌损伤,改善心肌缺血。
| [1] | Madder RD, Reynolds JC. Multidisciplinary management of the post–cardiac arrest patient[J]. Cardiol Clin, 2018, 36(1): 85-101. DOI:10.1016/j.ccl.2017.08.005 |
| [2] | 胡春林, 夏金明, 魏红艳, 等. 乌司他丁对心肺复苏后兔脑损伤和心功能的影响[J]. 中华急诊医学杂志, 2012, 21(1): 12-17. DOI:10.3760/cma.j.issn.1671-0282.2012.01.003 |
| [3] | Asgharzadeh F, Bargi R, Hosseini M, et al. Cardiac and renal fibrosis and oxidative stress balance in lipopolysaccharide-induced inflammation in male rats[J]. ARYA Atheroscler, 2018, 14(2): 71-77. DOI:10.22122/arya.v14i2.1550 |
| [4] | Bhakthavatsala Reddy C, Cyriac C, Desle HB. Role of "Ischemia Modified Albumin" (IMA) in acute coronary syndromes[J]. Indian Heart J, 2014, 66(6): 656-662. DOI:10.1016/j.ihj.2014.12.005 |
| [5] | 陈鑫, 聂时南. 亚低温治疗对心肺复苏后心功能不全的影响研究[J]. 临床急诊杂志, 2014, 15(12): 768-772. DOI:10.13201/j.issn.1009-5918.2014.12.023 |
| [6] | Gebhard W, Hoehstrasser K. Inter-d-trypsin inhibitor, and its close relatives[M]. Barrett AJ, Salvesen G. Proteinase Inhibitors.Amsterdam: Elsevier.1986: 375-388. |
| [7] | 温汉春, 朱继金. 心肺复苏过程中的脑保护策略研究进展[J]. 广西医学, 2012, 34(6): 771-772. DOI:10.3969/j.issn.0253-4304.2012.06.041 |
| [8] | 陈凤英, 廉明. 乌司他丁对猪心肺复苏后脑组织保护的研究[J]. 中华急诊医学杂志, 2017, 21(11): 1279-1283. DOI:10.3760/cma.j.issn.1671-0282.2017.11.011 |
| [9] | 武军元, 李春盛. 应用程控刺激的心脏骤停模型[J]. 中华急诊医学杂志, 2008, 17(10): 1063-1065. DOI:10.3760/cma.j.issn.1671-0282.2008.10.014 |
| [10] | Liu SY, Xu JF, Gao YZ, et al. Multi-organ protection of ulinastatin in traumatic cardiac arrest model[J]. World J Emerg Surg, 2018, 13(1): 51. DOI:10.1186/s13017-018-0212-3 |
| [11] | Chen HM, Huang HS, Ruan L, et al. Ulinastatin attenuates cerebral ischemia-reperfusion injury in rats[J]. Int J Clin Exp Med, 2014, 7(5): 1483-1489. |
| [12] | Wan X, Xie X, Gendoo Y, et al. Ulinastatin administration is associated with a lower incidence of acute kidney injury after cardiac surgery: a propensity score matched study[J]. Crit Care, 2016, 20: 42. DOI:10.1186/s13054-016-1207-7 |
| [13] | Guan L, Liu H, Fu P, et al. The protective effects of trypsin inhibitor on hepatic ischemia-reperfusion injury and liver graft survival[J]. Oxidative Med Cell Longev, 2016, 2016: 1429835. DOI:10.1155/2016/1429835 |
| [14] | Schroeder DC, Maul AC, Mahabir E, et al. Evaluation of small intestinal damage in a rat model of 6 minutes cardiac arrest[J]. BMC Anesthesiol, 2018, 18: 61. DOI:10.1186/s12871-018-0530-8 |
| [15] | Niemann JT, Garner D, Lewis RJ. Tumor necrosis factor-α is associated with early postresuscitation myocardial dysfunction[J]. Crit Care Med, 2004, 32(8): 1753-1758. DOI:10.1097/01.ccm.0000132899.15242.d3 |
| [16] | Wang Y, Branicky R, Noë A, et al. Superoxide dismutases: Dual roles in controlling ROS damage and regulating ROS signaling[J]. J Cell Biol, 2018, 217(6): 1915-1928. DOI:10.1083/jcb.201708007 |
| [17] | Papac-Milicevic N, Busch CJ, Binder CJ. Malondialdehyde epitopes as targets of immunity and the implications for atherosclerosis[J]. Adv Immunol, 2016, 131: 1-59. DOI:10.1016/bs.ai.2016.02.001 |
 2019, Vol. 28
2019, Vol. 28




