2 江西省九江学院附属医院外科 332000;
3 中日友好医院急诊科,北京 100029
2 Department of plastic surgery; Affiliated Hospital of Jiujiang University, Jiujiang, 332000, China;
3 Department of Emergency Medicine, China-Japan Friendship Hospital, Beijing, 100029, China
对血流动力学不稳定患者的容量状态判断是很关键、但很有难度的问题。足够的血管内容量是使用血管活性药物的前提条件,但过多的容量又会造成肺水肿等不良反应。常规的静态评估指标如中心静脉压、肺动脉楔压目前被认为不能很好地反应患者的容量状态。而动态指标如每搏输出量变异率和脉压变异率又基本仅对呼吸机控制通气的患者适用。被动抬腿实验(passive leg raising,PLR)通过让下肢静脉血液迅速回流,模拟了快速输液的过程,能迅速增加前负荷,如果患者有容量反应,心搏量(stroke volume,SV)就会明显增加。不论患者是否机械通气,PLR都能很好地预测患者的容量反应[1]。常规的PLR观察指标脉压变化率(pulse pressure change,ΔPP)和心搏量变化率(ΔSV)等在急诊应用都有许多局限性。本实验旨在评价用无创超声心输出量监测仪的主动脉血流速度时间积分功能(velocity time integral,VTI)观察PLR后患者的主动脉血流状况变化,判断其是否能应用于急诊患者的PLR,预测急诊患者的容量反应。
1 资料与方法 1.1 一般资料本实验前瞻性地研究从2014年10月至2016年10月北京协和医院急诊科抢救室和EICU收治的感染性休克或急性胰腺炎患者。患者的入组标准:(1)患者存在以下至少一项组织灌注不足的征象,包括:急性循环衰竭(收缩压小于90 mmHg或较前下降40 mmHg);尿量小于0.5 mL/kg至少1 h;心率增快HR大于100次/min);皮肤花斑。(2)非机械通气;(3)有心电监测;(4)有脉搏波形指示的连续心输出量(pulse indicated continuous cardiac output, PiCCO)监测。患者的排除标准:(1)有持续的心律失常;(2)USCOM不能获得满意图像;(3)患者有重度主动脉瓣关闭不全;(4)已有明确血容量过多的临床表现。
1.2 患者及设备准备所有患者置入中心静脉导管(颈内静脉或锁骨下静脉)和外周动脉导管(股动脉)进行PiCCO监测,采用热稀释方法测定心输出量,自中心静脉注射15 ml小于8℃的生理盐水,描记热稀释曲线,计算得到心输出量指数(Cardiac Output Index,CI)、心搏量(SV)等。收缩压和舒张压的差值为脉压(PP)。同时使用USCOM测得各时间点的VTI。
1.3 实验步骤第一步(基线1):患者半卧位,床头抬高30°-45°,测量基线水平参数。
第二步(PLR):患者床头放平,下肢抬高30°-45°持续1 min,测量PLR水平的参数。计算得到VTI较前增加率ΔVTIplr及PP较前增加率ΔPP。
第三步:患者下肢和床头回到基线体位5 min,得到基线2水平。
测量参数后,给予扩容:患者在30 min内静脉输注生理盐水500 mL,然后收集容量反应的相关数据。静脉输液后患者PiCCO监测的SV较基线2变化率(ΔSV)大于15%认为容量反应阳性,反之为容量反应阴性。同时通过USCOM得到VTI较基线2变化率(ΔVTIve)。
因为血流动力学参数在呼吸时会出现变化[2],观察10次连续心搏,包括至少一次呼吸,记录患者每个状态的VTI、PP、SV在呼吸过程中的最低值。每个血流动力学测量在最初的5 min内完成。VTI、PP、SV变化率(ΔVTIplr、ΔVTIve、ΔPP、ΔSV)用如下公式计算:变化率Δ(%) =100×(PLR后–基线)/基线,或Δ(%) =100×(扩容后–基线)/基线。
1.4 统计学方法应用SPSS 19统计软件分析。计量资料采用均数±标准差(Mean±SD)表示。两组间的计量资料比较采用配对t检验;相关性分析采用Spearman相关。以P < 0.05为差异有统计学意义。受试者工作曲线(receiver- operating characteristic curves ROC曲线)用Hanley-McNeil法得到,ΔPP和ΔVTI的阈值用最佳Youden指数法得到,Youden指数=敏感性+特异性-1。
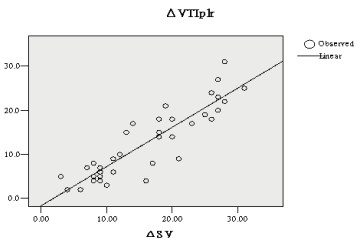
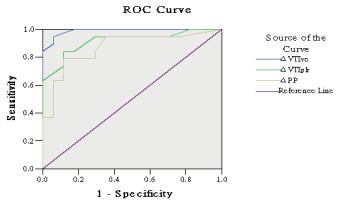
2 结果在研究期间,总计有36例患者满足入组条件。男性21例,女性15例,年龄(59±32)岁,最小年龄21岁,最大年龄89岁。每例患者只入组第一次的PLR和补液试验,其中容量反应阳性患者19例,容量反应阴性患者17例。所有患者获得了心率、血压,PiCCO测定的SV、CI及USCOM测定的VTI(表 1)。所有患者PLR后HR较基线1水平差异无统计学意义,而SV、CI、VTI较基线1都有显著升高(P < 0.05)。容量反应阳性患者的PP在PLR后较基线1水平有显著升高(P < 0.05),而容量反应阴性患者的PP升高不显著。所有患者PLR后的VTI变化ΔVTIplr为(12.8±8.1)%,补液后的VTI变化ΔVTIve为(16.6±8.0)%,PLR后的PP变化ΔPP为(11.1±7.7)%。ΔVTIplr和ΔSV之间的相关关系分析显示Spearman相关系数r=0.888(P < 0.01),两组指标之间存在显著的正相关关系(图 1)。ΔVTIve、ΔVTIplr及ΔPP在所有患者中对于预测容量反应的ROC曲线如图 2:ΔVTIve在 > 15%时的敏感性为94.7%,特异性为94.1%,曲线下面积0.989;ΔVTIplr在 > 12%时敏感性为84.2%,特异性为88.2%,曲线下面积0.916;ΔPP在 > 10.5%时的敏感性为78.9%,特异性为88.2%,曲线下面积0.870。
|
| r=0.888, p < 0.01 图 1 ΔVTIplr与ΔSV的相关分析 Fig 1 correlation between the patients' ΔVTIplr and ΔSV |
|
|
|
| 图 2 ΔVTIve、ΔVTIplr及ΔPP在所有患者中对于预测容量反应的ROC曲线 Fig 2 ROC curves for predicting capacity response in all patients: Δ VTIve, ΔVTIplr and ΔPP |
|
|
| 指标 | 基线1 | PLR后 | 基线2 | 扩容后 |
| HR, (次/min) | ||||
| 容量反应(+) | 107±24 | 106±27 | 107±21 | 105±19b |
| 容量反应(-) | 109±26 | 108±34 | 108±28 | 107±22b |
| PP, (mmHg) | ||||
| 容量反应(+) | 57±11 | 60±12a | 56±12 | 62±20b |
| 容量反应(-) | 54±13 | 56±14 | 55±11 | 59±24b |
| CI, (L/min·m2) | ||||
| 容量反应(+) | 3.12±1.23 | 3.29±1.42a | 3.13±1.07 | 3.35±1.62b |
| 容量反应(-) | 3.34±1.07 | 3.47±1.12a | 3.32±1.12 | 3.67±1.32b |
| SV, (ml) | ||||
| 容量反应(+) | 42±12 | 45±11a | 42±11 | 51±12b |
| 容量反应(-) | 46±13 | 48±10a | 45±12 | 49±11b |
| VTI, (cm) | ||||
| 容量反应(+) | 21±10 | 23±13a | 21±12 | 26±16b |
| 容量反应(-) | 22±15 | 23±16a | 21±14 | 24±17b |
| 注:容量反应(+)组n=19;容量反应(-)组n=17,PLR后与基线1状态比较,aP < 0.05;补液后与基线2比较, bP < 0.05 | ||||
容量判断在危重患者的治疗中是一个永恒的话题,容量不足会导致患者暴露于氧供不足和休克的危险;而容量过多则是危重患者病死率增加的独立危险因素[3]。现有的预测患者容量反应的指标有很多,包括经典的有创方法如肺动脉漂浮导管,微创方法如PICCO,无创方法如超声心动、USCOM,以及一些动态监测方法如补液试验、PLR。但是没有一种为公认的最佳方法。目前国内外对于容量监测的方法多是因地制宜,综合应用。
PLR是一种通过让下肢静脉血液迅速回流而短暂性增加回心血量的方法[4],大约能募集300 mL左右的下肢血液。PLR被认为是安全的“自体补液实验”,一旦患者下肢放平回到正常位置,补液作用就会逆转,而且即使下肢抬高时间偏长一些也不会有持续的补液作用。因其使用相对方便、安全性高得到大家的关注,持续地成为研究的热点[5-6],而且被越来越多地尝试用于急诊[7]。但目前限制其在急诊应用的一个很大的问题在于,判断PLR效果的经典观察指标为ΔPP [8],而ΔPP需要获得有创血压,有一定创伤,也很难实时得到结果,在急诊使用非常困难;近年研究较多的观察指标是超声心动的主动脉血流速度或SV变化[9]。而超声心动对急诊医师来说技术难度很高,同样难以实施。因此找到一个适合急诊的PLR观察指标显得尤为重要。
USCOM是一种非常易于上手的多普勒超声无创技术测定心输出量的仪器。在2001年最早应用于临床,它主要依赖连续多普勒超声技术实时描记主动脉或肺动脉血流频谱,并根据得到的频谱图形计算患者的心输出量和其他血流动力学参数。所用探头的频率为2.0 MHz,探查主动脉血流频谱的窗口位于胸骨上。一旦获得满意血流频谱,则可以通过主动脉流出道的流速波形获得VTI,根据SV = S×VTI计算得到每搏量,从而得到心输出量,其中S为主动脉瓣口横截面积,VTI代表射血的距离。USCOM的使用范围较广[10-11],其效果被许多临床试验所评估,其中和经典的热稀释法以及食道超声法比较的研究较多,但结果差异较大,有的认为相关性可以接受[12],有的则认为相关性差[13-14]。认为相关性差的多数实验发现,其误差的主要原因是USCOM估测的主动脉瓣口横截面积和超声心动实际测量的横截面积的相关性差。USCOM所使用的瓣口横截面积应用患者身高通过Nidorf回归方程进行计算得到[15],而Nidorf回归方程是从健康志愿者的数据分析得到,因此USCOM所使用的主动脉瓣口横截面积为估测面积而并非患者的实际面积。由于存在个体差异、基础心脏病等问题,导致USCOM所使用的主动脉瓣口横截面积与实际值之间存在差异,在最终得到的心指数结果与实际结果之间存在差异就不可避免了。虽然USCOM测得的SV绝对数不十分令人满意,但在观察PLR效果时以及判断容量反应时往往使用的是SV的变化比例ΔSV%,而非绝对的SV,考虑到患者短时间内主动脉瓣口横截面积不会有明显变化,ΔSV%从理论上是和ΔVTI%等同的。本研究试验性使用USCOM所测得的ΔVTI%作为观察PLR效果和容量反应判断的指标,既避免了USCOM测SV的缺限,又没有用心脏彩超获得VTI的技术难度,为容量反应判断的无创监测提供了新的可选方法。
本研究发现,PLR后患者的HR不论在有容量反应的患者还是在无容量反应的患者,差异均无统计学意义,说明用临床上最容易获得的指标HR来判断PLR的容量反应效果很差。PLR后所有患者的VTI较输液前都有显著变化,ΔVTIplr和患者输液后的SV变化ΔSV有很好的线性相关关系。ΔVTIplr在 > 12%时较ΔPP在 > 10.5%时对患者容量反应的判断特异性相当,敏感性更好,ROC曲线下面积也较ΔPP大。说明用USCOM测得的ΔVTI是一个敏感性和特异性都较高的指标,用VTI在PLR前后的变化评估PLR的反应效果好。在我们的研究中ΔVTI表现优于经典指标ΔPP,这个结果和用食道超声测出的主动脉流速的结果有些类似[9],但很明显,通过USCOM监测ΔVTI完全无创,而食道超声有一定创伤,同时USCOM也明显更易于急诊医师掌握,因此笔者认为USCOM监测ΔVTIplr有很好的急诊应用前景。
另一方面,在急诊使用PiCCO或漂浮导管得到SV费时、有创、价格昂贵[16],而USCOM所得到的SV准确性又难以保证,但目前公认的判断容量反应的标准有都是以补液后ΔSV大于15%来判断,能否有其他的方法替代ΔSV是我们关心的问题。能否用USCOM测得的ΔVTI替代ΔSV呢?为了进一步检测USCOM测得的ΔVTI的效果,本研究在补液后不仅计算了PiCCO所得的SV变化率ΔSV,也计算了相应的VTI变化率ΔVTIve,发现ΔVTIve和ΔSV结果非常接近,ΔVTIve在 > 15%时的敏感性和特异性都接近95%。从本研究可以发现,在急诊的容量反应判断中,使用USCOM测得的ΔVTIve是否大于15%来判断患者的容量反应准确性是有保障的。
综上所述,不论是在被动抬腿实验中,还是在补液试验中,用USCOM无创多普勒超声获得的血流速度时间积分VTI作为观察指标,都能准确地评估患者的容量反应。这种方法使用方便,适用于急诊,值得进一步进行更大规模的临床试验进行印证、推广。
| [1] | Cherpanath TGV, Hirsch A, Geerts BF, et al. Predicting fluid responsiveness by passive leg raising[J]. Criti Care Med, 2016, 44(5): 981-991. DOI:10.1097/ccm.0000000000001556 |
| [2] | Soubrier S, Saulnier F, Hubert H, et al. Can dynamic indicators help the prediction of fluid responsiveness in spontaneously breathing critically ill patients[J]. Intensive Care Med, 2007, 33(7): 1117-1124. DOI:10.1007/s00134-007-0644-9 |
| [3] | Marik PE. Iatrogenic salt water drowning and the hazards of a high central venous pressure[J]. Ann Intensive Care, 2014, 4: 21. DOI:10.1186/s13613-014-0021-0 |
| [4] | Monnet X, Cipriani F, Camous L, et al. The passive leg raising test to guide fluid removal in critically ill patients[J]. Ann Intensive Care, 2016, 6(1): 46. DOI:10.1186/s13613-016-0149-1 |
| [5] | Krige A, Bland M, Fanshawe T. Fluid responsiveness prediction using Vigileo FloTrac measured cardiac output changes during passive leg raise test[J]. J Intensive Care, 2016, 6(4): 63. DOI:10.1186/s40560-016-0188-6 |
| [6] | Vistisen ST, Enevoldsen J, Scheeren TWL. Can passive leg raising be considered the gold standard in predicting fluid responsiveness?[J]. Am J Respir Crit Care Med, 2017, 195(8): 1075-1076. DOI:10.1164/rccm.201701-0060LE |
| [7] | Li W, Yu XZ, Xu J. An indispensable procedure to complete passive leg raising[J]. Ann Emerg Med, 2016, 68(3): 394-395. DOI:10.1016/j.annemergmed.2016.04.009 |
| [8] | Boulain T, Achard JM, Teboul JL, et al. Changes in BP induced by passive leg raising predict response to fluid loading in critically ill patients[J]. Chest, 2002, 121(4): 1245-1252. DOI:10.1378/chest.121.4.1245 |
| [9] | Monnet X, Rienzo M, Osman D, et al. Passive leg raising predicts fluid responsiveness in the critically ill[J]. Crit Care Med, 2006, 34(5): 1402-1407. DOI:10.1097/01.CCM.0000215453.11735.06 |
| [10] | Vinayagam D, Patey O, Thilaganthan B, et al. A cross comparison study of USCOM?and transthoracic echocardiography in pregnancy[J]. Ultrasound Obstet Gynecol, 2017, 49(1): 32-38. DOI:10.1002/uog.15915 |
| [11] | Critchley LAH, Huang L. USCOM:window to the circulation:utility of supra-sternal Doppler in an elderly anaesthetized patient for a robotic cystectomy[J]. J Clin Monit Comput, 2014, 28(1): 83-93. DOI:10.1007/s10877-013-9499-5 |
| [12] | McNamara H, Barclay P, Sharma V. Accuracy and precision of the ultrasound cardiac output monitor (USCOM 1A) in pregnancy:comparison with three-dimensional transthoracic echocardiography[J]. Br J Anaesth, 2014, 113(4): 669-676. DOI:10.1093/bja/aeu162 |
| [13] | Thom O, Taylor DM, Wolfe RE, et al. Comparison of a supra-sternal cardiac output monitor (USCOM) with the pulmonary artery catheter[J]. Br J Anaesth, 2009, 103(6): 800-804. DOI:10.1093/bja/aep296 |
| [14] | van den Oever HLA, Murphy EJ, Christie-Taylor GA. USCOM (ultrasonic cardiac output monitors) lacks agreement with thermodilution cardiac output and transoesophageal echocardiography valve measurements[J]. Anaesth Intensive Care, 2007, 35(6): 903-910. DOI:10.1177/0310057x0703500608 |
| [15] | Nidorf SM, Picard MH, Triulzi MO, et al. New perspectives in the assessment of cardiac chamber dimensions during development and adulthood[J]. J Am Coll Cardiol, 1992, 19(5): 983-988. DOI:10.1016/0735-1097(92)90282-r |
| [16] | Lamia B, Kim HK, Severyn DA, et al. Cross-comparisons of trending accuracies of continuous cardiac-output measurements:pulse contour analysis, bioreactance, and pulmonary-artery catheter[J]. J Clin Monit Comput, 2018, 32(1): 33-43. DOI:10.1007/s10877-017-9983-4 |
 2019, Vol. 28
2019, Vol. 28




