营养支持是危重患者综合救治过程中非常重要的内容,合理的营养支持能够促进危重症患者的康复,缩短住院时间和费用,以及降低并发症和住院病死率[1]。近年来,早期肠内营养因其能够避免因肠道细菌移位所致的多器官功能障碍综合征的发生,并有助于改善肠黏膜的结构和功能,维持肠道的完整性,预防应激性溃疡,而受到各大指南的推荐[2-4]。肠内营养支持剂量选择主要包括两种形式:滋养型喂养(trophic feeding)指以41.84~83.68 kJ(10~20 kcal)/h或10~20 mL/h的输注速率给予患者肠内营养支持治疗,一般热卡量为目标量的40%~60%。该喂养方式能够有效防止黏膜的萎缩,患者耐受性较好,但并不能达到全量营养支持所取得的临床效果[5-8];全喂养(full feeding)指以25~30 kcal/h速度开始,快速达到目标营养量,要求热卡量为目标量的70%~100%。该方式能够保证危重患者的营养需求,但危重患者由于严重的应激因素存在,大量营养物质进入体内,可能会给机体代谢造成负担,出现营养物质代谢异常或血糖水平的紊乱,反而会造成机体功能障碍[9-11]。目前针对危重患者最优化卡路里摄入量仍没有一致的认识,本研究旨在通过Meta分析比较滋养型喂养和全喂养在危重患者病死率、ICU入住时间、院内感染、胃肠道耐受性等方面的差异,为危重患者营养支持实践提供指导意义。
1 资料与方法 1.1 文献纳入和排除标准 1.1.1 研究类型随机对照试验(RCT)。
1.1.2 研究对象研究对象为18周岁以上,入住ICU需进行肠内营养支持的危重患者,种族、国籍、性别不限。
1.1.3 干预措施干预组采用滋养型喂养,指以41.84~83.68 kJ(10~20 kcal)/h或10~20 ml/h的输注速率给予患者肠内营养支持治疗。对照组采用全喂养,指以25~30 kcal/h速度开始,快速达到目标营养量。
1.1.4 结局指标主要指标:①病死率;②住院时间。次要指标:①院内感染发生率;②机械通气时间;③胃肠道耐受性。
1.2 文献检索策略计算机检索中英文数据库Cochrane图书馆、PubMed、Web of Science、Scopus、CINAHL、中国生物医学文献数据库(CBM)、中国知网(CNKI)、万方数据库,查找关于肠内营养喂养剂量选择方式相关的研究文献,检索时限均从建库至2017年6月,检索词为主题词和自由词结合,英文检索词包括critical care/intensive care/critical illness/ICU、enteral nutrition、trophic feed*/ underfeeding/insufficient feed*/bolus feed*、full feed*/fullfeeding/standard feed*/ aggressive feed*/target feed*/intensive feed*,中文检索词包括:肠内营养/鼻饲、危重患者/重症患者/ICU、滋养型喂养/低剂量喂养/小剂量喂养、全喂养/充分喂养。此外,采用滚雪球法对纳入文献的参考文献进行手工检索。
1.3 文献筛选所有研究者接受完整的系统评价培训。由2名研究者独立进行文献检索,按纳入与排除标准筛选文献,并交叉核对:首先阅读文题,如符合纳入标准,则进一步阅读摘要、全文。如遇分歧,则通过讨论解决,若仍存在分歧由第3名研究者协调解决。
1.4 质量评价 1.4.1 文献偏倚风险评估由2名研究者参照Cochrane系统评价手册偏倚风险评估标准[12]独立评估后进行交叉核对,如有分歧,则与第3名研究者共同讨论并达成一致。评价标准包括:①随机分配方案的产生;②分配方案隐藏;③对患者和医生实施盲法;④对结果评价实施盲法;⑤结果数据的完整性;⑥无选择性报告结果;⑦无其他偏倚来源。每个条目以“是”“否”“不清楚”“未应用”,进行评判。完全满足各项标准,发生偏倚可能性最小;部分满足各项标准,发生偏倚可能性为中度;完全不满足各项标准,发生偏倚可能性为高度。
1.4.2 证据的整体质量评价采用GRADE系统推荐分级方法[13],证据质量分级如下:①高质量:进一步研究不可能改变该疗效评估结果的可信度;②中等质量:进一步研究很可能影响该疗效评估结果的可信度,且可能改变该评估结果;③低质量:进一步研究极有可能影响该疗效评估结果的可信度,且该评估结果很可能改变;④极低质量:任何疗效评估结果都很不确定。虽然基于RCT得出的证据一开始被定为高质量,但研究对该类证据的信心可能会因为下面5个因素而降低:①研究的局限性;②研究结果的不一致;③间接证据;④结果不精确;⑤报告有偏倚。
1.5 资料提取按照制定的数据提取表提取资料,提取内容主要包括:①基本特征(作者、发表年限、国家);②研究类型;③研究对象;④样本量;⑤试验组和对照组的干预措施;⑥干预时间;⑦结局指标等。缺乏的资料通过电话或信件与作者联系尽量补充。
1.6 统计学方法采用RevMan5.3统计软件对文献进行Meta分析,首先对研究资料进行异质性检验,若异质性检验P > 0.1,I2≤50%,认为研究间具有同质性,选择固定效应模型计算合并量。在异质性较大时进行敏感性分析和亚组分析,寻找异质性来源,若结果仍不同质选择随机效应模型计算合并量。计量资料采用标准化均数差(SMD)或加权均数差(WMD);计数资料采用比值比(RR)为疗效分析统计量。所有效应量以95%可信区间(CI)表示。发表偏倚检测使用漏斗图。
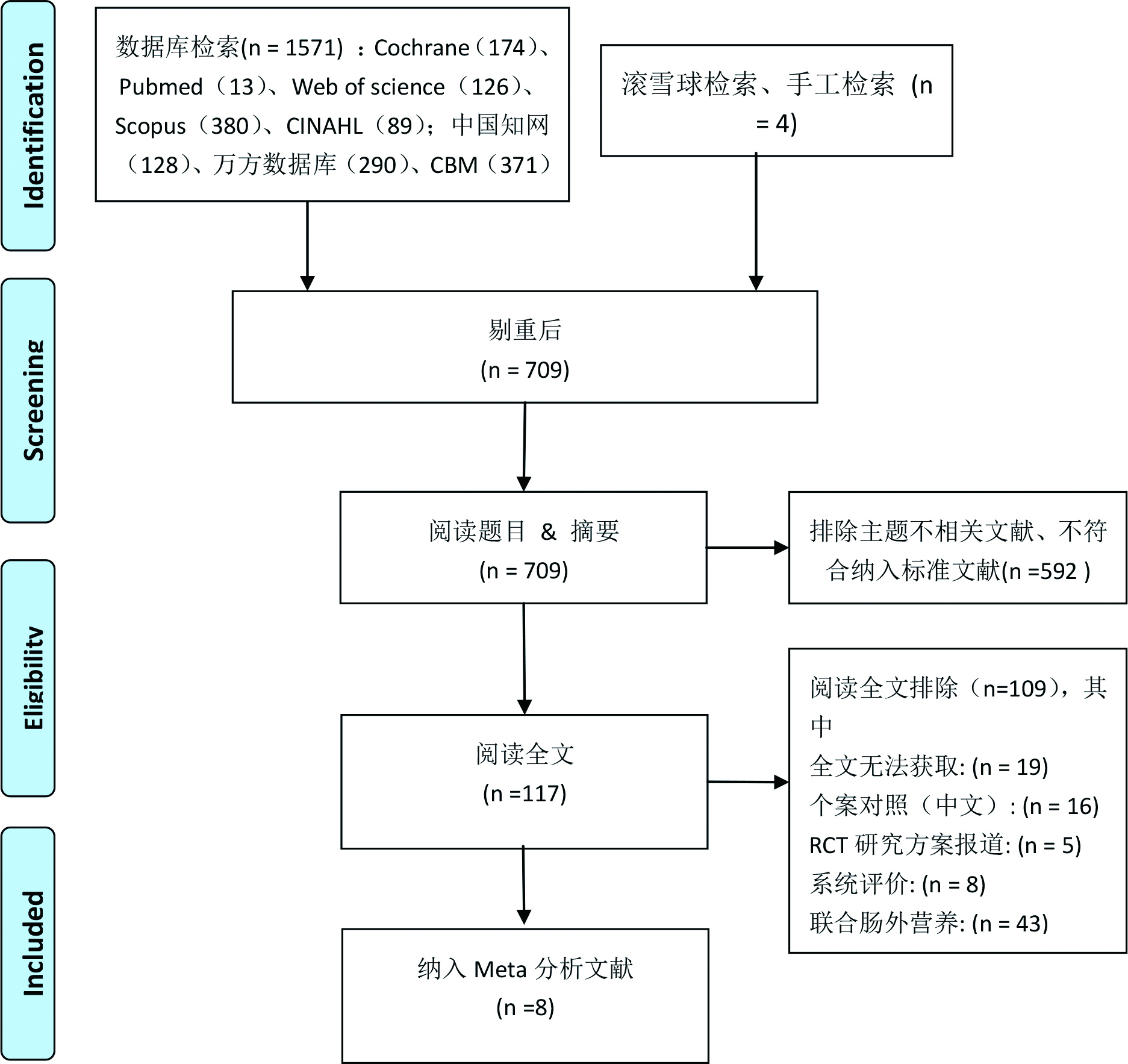
2 结果 2.1 文献检索结果通过文献数据库初检获得1 571篇文献(中文789篇,英文782篇),其他途径补充获得4篇英文文献,剔除重复文献得709篇,阅读题目和摘要,排除不符合纳入排除标准的文献592篇,共117篇文献可能符合入选标准。进一步阅读全文后,排除109篇最终纳入文献8篇,中文1篇,英文7篇。文献检索流程见图 1。
|
| 图 1 文献检索与筛选流程图 Figure 1 Literature screening flow |
|
|
严格按照纳入标准筛选文献,最终共纳入8项[8, 14-20]随机对照试验(RCT),研究来自德国(研究时间:2014)、美国(2011、2012)、法国(2008)、沙特阿拉伯(2011、2015)、哥伦比亚(2014)和中国(2014),共计2 713例患者。均为滋养型喂养方式和全喂养相比,干预时间从4 d至9 d不等。纳入文献的一般情况见表 1,营养支持情况见表 2。
| 纳入研究 | 研究设计 | 研究对象 | 样本量 (UF / FF) |
性别(男) (UF / FF) |
年龄(岁) (UF / FF) |
BMI(kg/m2) (UF / FF) |
疾病危重度 (UF / FF) |
| Petros 2014 | RCT | ICU患者 | 46/54 | 32/34 | 67.6±11.5/64.3±11.5 | 28.6±6.5/27.1±6.8 | APACHEⅡ: 30.5±8.5/27.7±8.4 |
| Desachy 2008 | RCT | ICU患者 | 50/50 | 31/38 | 64±13/58±19 | 27±5/25±3 | SAPSⅡ: 40.0±11.0/42.0±17.0 |
| Rice 2012 | RCT | ICU患者 | 508/492 | 267/243 | 52±16/52±17 | 29.9±7.8/30.4±8.2 | APACHEⅢ: 92±28/90±27 |
| Arabi 2015 | RCT | ICU患者 | 448/446 | 292/282 | 50.2±19.5/50.9±19.4 | 29.0±8.2/29.7±8.8 | APACHEⅡ: 21±7.9 |
| Arabi 2011 | RCT | ICU患者 | 120/120 | 86/78 | 50.3±21.3/51.9±22.1 | 28.5±7.4/28.5±8.4 | APACHEⅡ: 25.2±7.5 |
| Rice 2011 | RCT | ICU患者 | 98/102 | 36/47 | 53±19/54±17 | 29.2±10.2/28.2±9.4 | APACHEⅡ: 26.9±8.1 |
| Rugeles 2014 | RCT | ICU患者 | 40/40 | 22/24 | 53.3±19.5/55.7±19.5 | 23.7±3.3/24.3±4.4 | APACHEⅡ: 13.9±4.8 |
| 林少华2014 | RCT | ICU患者 | 50/49 | 26/25 | 52±4/50±6 | 30±8/29±7 | APACHEⅡ: 30±9 |
| 注:UF,滋养型喂养;FF,全喂养 | |||||||
| 纳入研究 | 喂养开始时间 | 卡路里需求 (UF / FF) |
卡路里摄入 (UF / FF) |
初始速度(mL/h) (UF / FF) |
递增速度(mL) (UF / FF) |
干预时间(d) (UF / FF) |
胃残留量标准(mL) | 结局指标 |
| Petros 2014 | < 24 h | 1 837±340/1 777±333e | 11.3±3.1/19.7±5.7f | NR | NR | 7/7 | 300 | a/b/d/e/f |
| Desachy 2008 | < 24 h | 1800±314/ 1 836±340e | 1 297±331/1 715±331e | 25/目标速率 | 25/24 h /开始即达到目标速率 | 4.7±2.0/5.3±1.9 | 300 | a/b/c/f |
| Rice 2012 | 0~72 h | NR | 400/1300e | 10~20/25 | 0 / 25/6 h | 6/6 | 400 | a/d/e/f |
| Arabi 2015 | NR | 1 822±377/1 842±370e | 835±297/1299±467e | 30/30 | 10/4 h / 10/4 h | 9.4±4.4/9.1±4.6 | 200 | a/b/c/d/e/f |
| Arabi 2011 | < 24 h | 1 833.0±335.8/1 767.6±311.3e | 1 066.6±306.1/1 251.7±432.5e | 30/30 | 10/12 h / 10/4 h | 7/7 | 150 | a/b/c/d/e |
| Rice 2011 | < 12 h | 1 570±225/1 608±277f | 300±149/1 418±686e | 10/25 | 0 / 25/6 h | 5.1±3.3/5.5±3.6 | 300 | a/d/e/f |
| Rugeles 2014 | NR | 15/25f | 12/14f | 15/25 | NR | NR | c/d | |
| 林少华2014 | < 48 h | 15-20/25-30f | 18.3±2.9/27.5±3.4f | 10/25 | 0 / 25/8 h | 7/7 | 200 | a/c/e/f |
| 注:UF,滋养型喂养;FF,全喂养;a整体病死率;b ICU病死率;c ICU入住时间;d机械通气时间;e院内感染率;f胃肠道不耐受性(指呕吐、反流、胃动力药使用、腹泻、便秘);e kcal/d; f kcal/(kg·d) | ||||||||
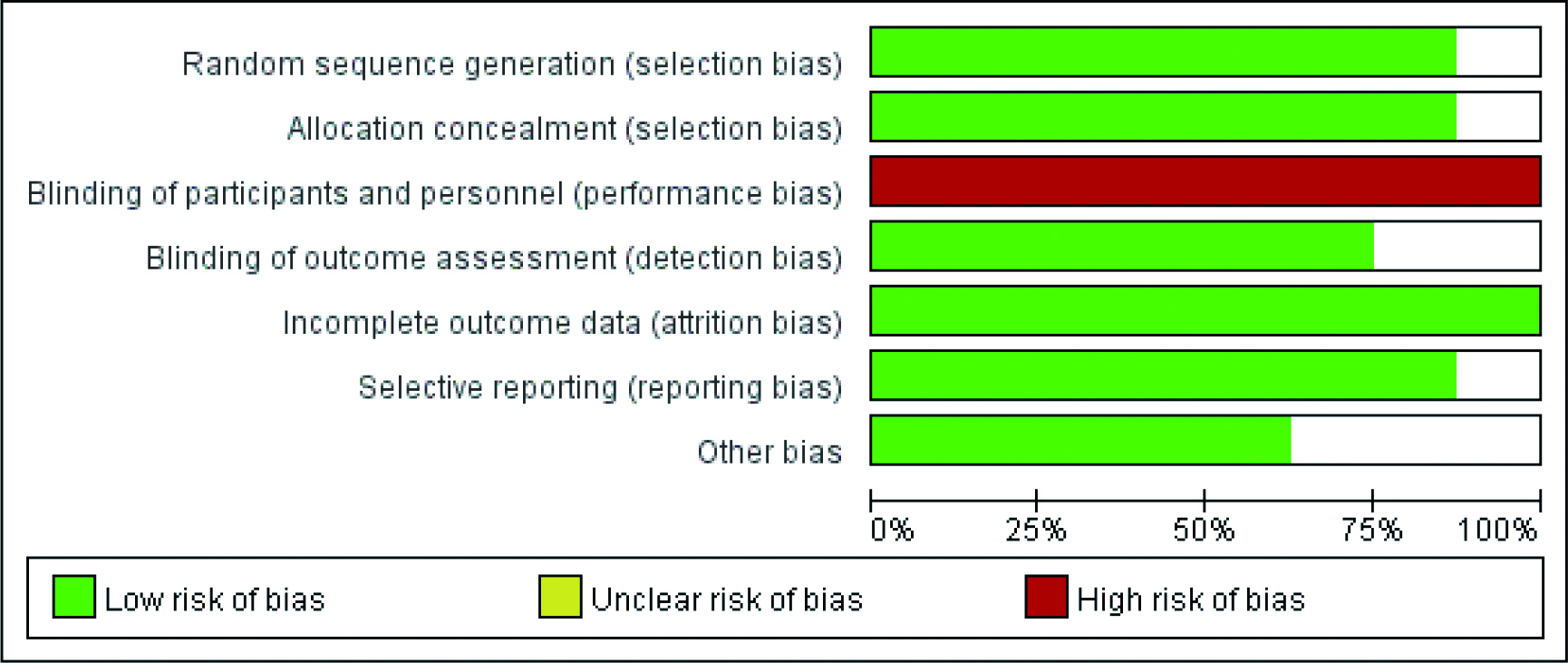
根据Cochrane系统评价手册偏倚风险评估标准,纳入研究的偏倚风险评价结果见图 2。纳入的8篇RCT中,对患者和医生实施盲法条目均较差,存在较高风险;所有研究对随机方法、分配隐藏、结果数据的完整和报告结果条目均较好;2篇研究未报道对评价者实施盲法。均处于低偏倚风险。
|
| 图 2 文献偏倚风险评估 Figure 2 Literature bias risk assessment |
|
|
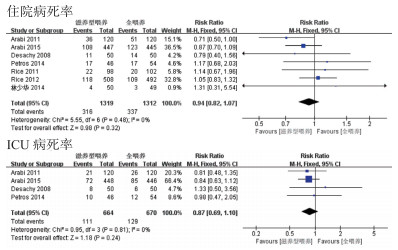
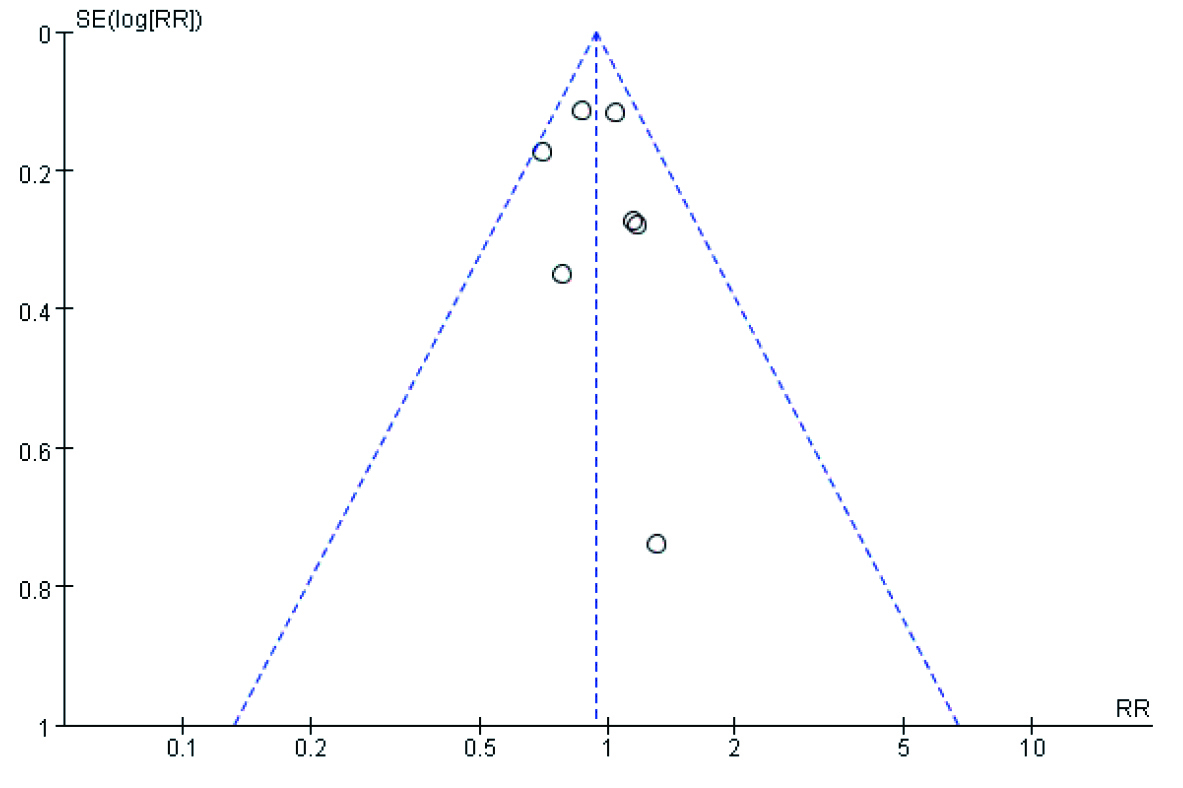
7篇[8, 14-18, 20]文献报道了滋养型喂养组与全喂养组住院病死率方面的差异,研究间不存在统计学异质性(P=0.48,I2=0%),采用固定效应模型行Meta分析(图 3),合并效应无统计学意义[RR=0.94, 95%CI: 0.82~1.07, P=0.32],提示滋养型喂养和全喂养相比,住院病死率差异无统计学意义。此7篇文献的漏斗图(图 4)较为对称理想,发表偏倚较小。其中4篇[8, 14-15, 17]研究报道了ICU病死率,研究间无统计学异质性(P=0.48,I2=0%),合并效应差异无统计学意义[RR=0.87, 95%CI: 0.69~1.10, P=0.24](图 3)。
|
| 图 3 病死率Meta分析 Figure 3 Mortality Meta analysis |
|
|
|
| 图 4 发表偏倚分析-漏斗图 Figure 4 Publication bias assessment |
|
|
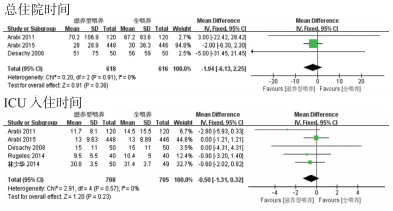
3篇文献[8, 15, 17]报道了研究中喂养方式对总住院时间的影响,研究间无统计学异质性(P=0.91,I2=0%),故采用固定效应模型行Meta分析(图 5),合并效应无统计学意义[SMD=-1.94, 95%CI:-6.13~2.25, P=0.36];5篇[8, 15, 17, 19, 20]研究对ICU入住时间进行比较,合并效应同样无统计学意义[SMD=-0.50, 95%CI:-1.31~0.32, P=0.23],显示滋养型喂养和全喂养在总住院时间和ICU入住时间方面均无差异。
|
| 图 5 住院时间Meta分析 Figure 5 The lengths of stay Meta analysis |
|
|
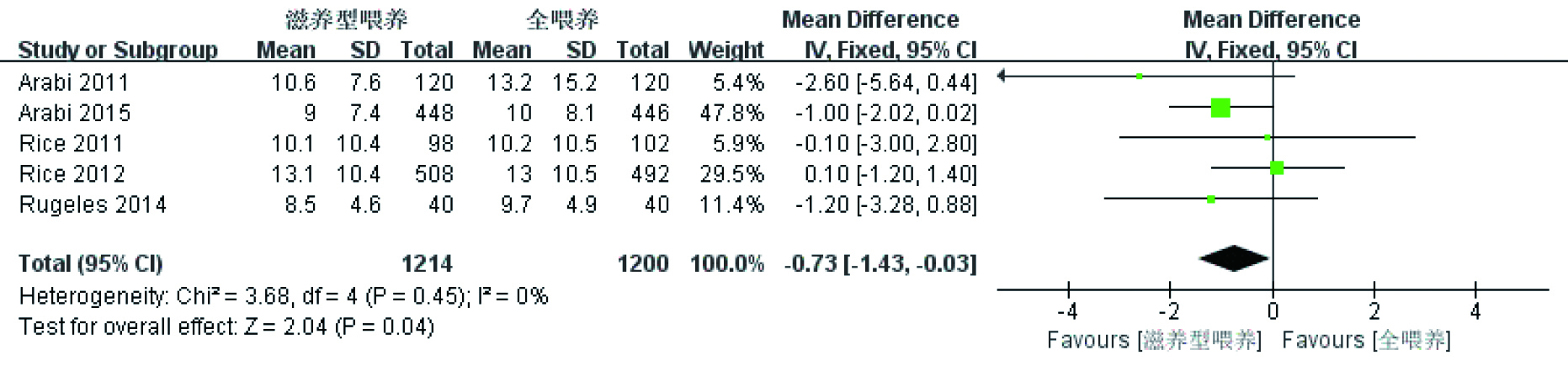
5篇[8, 16-19]研究以机械通气时间为结局指标,比较滋养型喂养和全喂养之间的差异,共包含2 214例研究对象,研究间无统计学异质性(P=0.45,I2=0%),采用固定效应模型(图 6),合并效应有统计学意义[SMD=-0.73, 95%CI:-1.43~-0.03, P=0.04],显示滋养型喂养有助于降低ICU患者的机械通气时间。
|
| 图 6 机械通气时间Meta分析 Figure 6 The mechanical ventilation time Meta analysis |
|
|
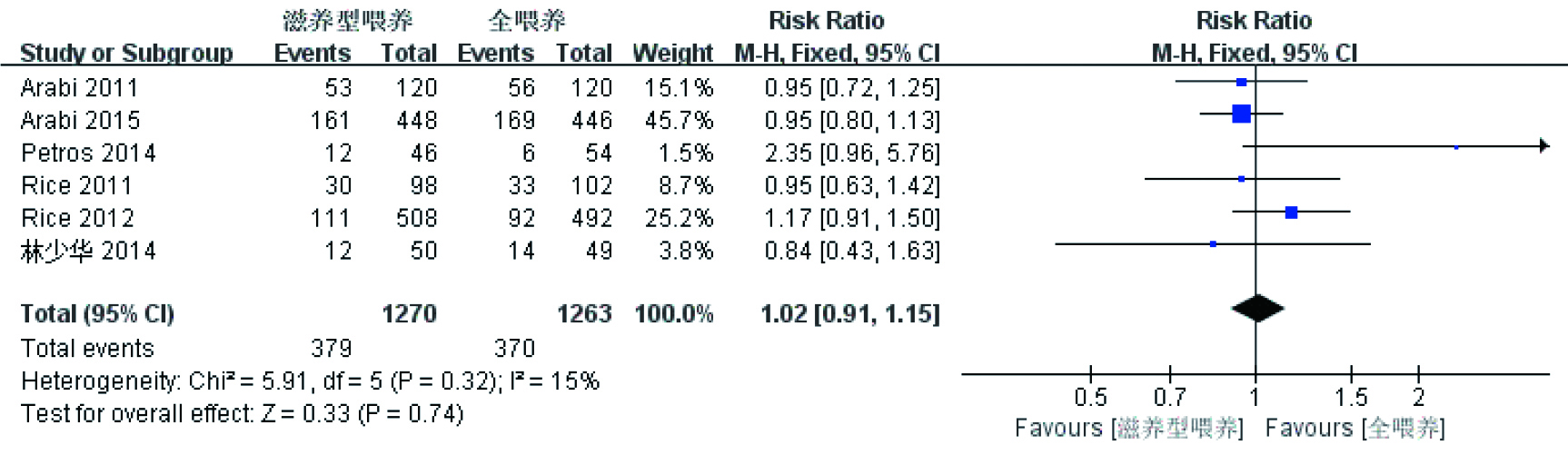
6篇研究[8, 14, 16-18, 20]采用院内感染的发生率作为结局指标,共纳入2 533名研究对象,研究间异质性较小(P=0.74,I2=15%),采用固定效应模型(图 7),合并效应量差异无统计学意义[RR=1.02, 95%CI: 0.91~1.15, P=0.74],显示滋养型喂养和全喂养相比,院内感染的发生率差异有统计学意义。
|
| 图 7 院内感染发生率Meta分析 Figure 7 Nosocomial infection rate Meta analysis |
|
|
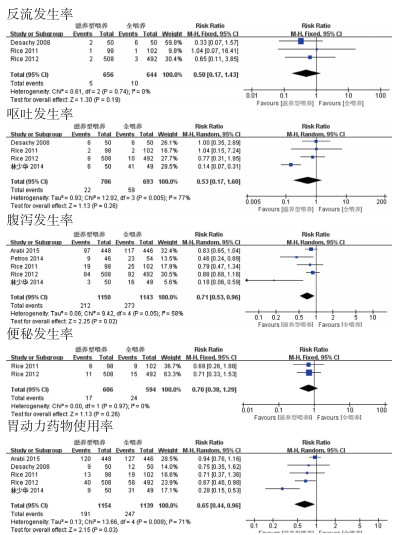
6篇研究报道了两种喂养方式在胃肠道耐受性方面的差异,包括反流、呕吐、腹泻、便秘、胃动力药使用; 在腹泻发生率[RR=0.71, 95%CI:0.53~0.96, P=0.02]和胃动力药物使用率[RR=0.65, 95%CI:0.44~0.96, P=0.03]这2个指标方面合并效应量有统计学意义,相比全喂养,滋养型喂养有助于降低ICU患者肠内营养期间腹泻的发生率和胃动力药的使用率。见图 8。
|
| 图 8 胃肠道耐受性Meta分析 Figure 8 Gastrointestinal tolerance Meta analysis |
|
|
通过对2个主要结局(病死率、住院时间)指标进行证据质量评价,结果显示均为中等质量级别证据,后续研究可能对本研究的效应估计产生影响。
3 讨论本次纳入8项RCT研究,偏倚风险评估中,对研究对象和实施者盲法均未做到,主要原因在于干预方法(喂养方式)需由实施者完成,无法实施盲法,同样研究对象可通过喂养量观察确定组别,但研究均详细报道了营养支持流程,因此能够保证干预方案准确实施。结果数据的完整指标符合率为100%,其他指标如随机方法描述、分配隐藏、结局指标测量和报告结果条目符合率均较高,报告质量较高。
近年来,重症患者的临床营养支持的重要性得到了广泛的认识和关注,早期肠内营养因其能够维持胃肠道黏膜结构与功能的完整性、减少细菌移位,已被证实能够显著降低并发症的发生率、缩短ICU住院时间,改善患者预后[21-22]。然而,危重患者早期肠内营养应该摄入多少能量并没有一致的认识。本研究采用病死率和住院时间作为主要结局指标,反映喂养方式对患者预后的影响,表明尽管滋养型喂养相比全喂养,合并效应量体现出病死率和住院时间降低的趋势,但差异无统计学意义,提示选择低卡路里摄入方式喂养并不影响患者的预后。
全喂养相比滋养型喂养,总热量摄入和单日喂养量均较高,意味着全喂养情况下,患者的胃肠道负荷较高,可能会出现一系列胃肠道不耐受症状。本系统评价将胃肠道耐受性定义为,包含反流、呕吐、腹泻、便秘、使用胃动力药物。图 8结果显示,滋养型喂养能够显著降低ICU患者腹泻发生率和胃动力药物的使用率,改善ICU患者的胃肠道耐受性。尽管滋养型喂养已经在反流、呕吐和便秘发生率下降方面已经表现出优势,但并未达到统计学差异,可能与各研究间评价指标的定义方式不同有关。研究表明:胃肠道不耐受症状往往与院内感染、机械通气时间延迟有关联[23],本研究也证实了这一点,通过将5篇研究合并,发现滋养型喂养能够显著降低ICU患者的机械通气时间。院内感染发生率合并效应量没有表现出统计学意义,可能与院内感染的发生是多重因素作用的结果,各研究对于发生院内感染的时间截点界定并不完全一致有关。
本研究纳入8篇文献,能量需求的测定均为间接方式,并未采用客观、量化的方式定量患者的营养摄入需求,且各研究采用的方式各异,是原文献报道最大的局限性,因此,对于本次Meta分析的结果因保持谨慎。同时,本研究仅检索到3篇国内相关临床研究,其中2篇由于设计、人群以及方法学质量不符合纳入标准,未纳入分析。危重患者的早期肠内营养理念引入国内不久,对于更深入的能量摄入剂量及组成等方面尚未引起足够的关注和重视。因此,本研究建议国内在借鉴喂养方式时,考虑国内外人群等方面差异,期待国内相关研究报道的出现,为临床工作提供更可靠的证据。
| [1] | 戚建巨, 叶立刚, 徐善祥, 等. 浙江省危重症营养治疗的医护认知的调查研究[J]. 中华急诊医学杂志, 2016, 25(10). DOI:10.3760/cma.j.issn.1671-0282.2016.10.024 |
| [2] | ESPEN. ESPEN Guidelines on Enteral Nutrition:Intensive care[J]. Clin Nutr, 2009, 28(4): 387-400. DOI:10.1016/j.clnu.2006.01.021 |
| [3] | Dhaliwal R, Cahill N, Lemieux M, et al. The Canadian critical care nutrition guidelines in 2013:an update on current recommendations and implementation strategies[J]. Nutr Clin Pract, 2014, 29(1): 29-43. DOI:10.1177/0884533613510948 |
| [4] | McClave SA, Taylor BE, Martindale RG, et al. Society of Critical Care Medicine. American Society for Parenteral and Enteral Nutrition.Guidelines for the Provision and Assessment of Nutrition Support Therapy in the Adult Critically Ill Patient:Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N.)[J]. JPEN J Parenter Enteral Nutr, 2016, 40(2): 159-211. DOI:10.1177/0148607109335234 |
| [5] | Barthel H, Steinert F. Stumpp Effect of 6-month calorie restriction on biomarkers of longevity, Metabolic adaptation, and oxidative stress in overweight individuals:a randomized controlled trial[J]. JAMA, 2006, 295(21): 1539-1548. DOI:10.1001/jama.295.13.1539 |
| [6] | Krishnan JA, Parce PB, Martinez A, et al. Caloric intake in medical ICU patients:consistency of care with guidelines and relationship to clinical outcomes[J]. Chest, 2003, 124(1): 297-305. DOI:10.1378/chest.124.1.297 |
| [7] | Braunschweig CA, Sheean PM, Peterson SJ, et al. Intensive nutrition in acute lung injury:a clinical trial (INTACT)[J]. JPEN J Parenter Enteral Nutr, 2015, 39(1): 13-20. DOI:10.1177/0148607114528541 |
| [8] | Arabi YM, Tamim HM, Dhar GS, et al. Permissive underfeeding and intensive insulin therapy in critically ill patients:a randomized controlled trial[J]. Am J Clin Nutr, 2011, 93(3): 569-577. DOI:10.3945/ajcn.110.005074 |
| [9] | O'Leary MJ, Ferrie S. Early or late parenteral nutrition in critically ill adults[J]. N Engl J Med, 2011, 365(19): 1841-1842. DOI:10.1056/NEJMc1110994 |
| [10] | Casaer MP, Wilmer A, Hermans G, et al. Role of disease and macronutrient dose in the randomized controlled EPaNIC trial:a post hoc analysis[J]. Am J Respir Crit Care Med, 2013, 187(3): 247. DOI:10.1164/rccm.201206-0999OC |
| [11] | Doig G S, Simpson F, Finfer S, et al. Effect of evidence-based feeding guidelines on mortality of critically ill adults:a cluster randomized controlled trial[J]. JAMA, 2008, 300(23): 2731-2741. DOI:10.1001/jama.2008.826 |
| [12] | Higgins, Julian PT. Cochrane handbook for systematic reviews of interventions[M]. Wiley-Blackwell, 2008. |
| [13] | BalshemH, HelfandaM, SchunemannHJ, 等. GRADE指南:证据质量分级[J]. 中国循证医学杂志, 2011, 11(4): 451-455. DOI:10.3969/j.issn.1672-2531.2011.04.017 |
| [14] | Petros S, Horbach M, Seidel F, et al. Hypocaloric vs normocaloric nutrition in critically ill patients:a prospective randomized pilot trial[J]. JPEN J Parenter Enteral Nutr, 2016, 40(2): 242. DOI:10.1177/0148607114528980 |
| [15] | Desachy A, Clavel M, Vuagnat A, et al. Initial efficacy and tolerability of early enteral nutrition with immediate or gradual introduction in intubated patients[J]. Intensive Care Med, 2008, 34(6): 1054-1059. DOI:10.1007/s00134-007-0983-6 |
| [16] | Rice TW, Wheeler AP, Thompson BT, et al. Initial Trophic vs Full Enteral Feeding in Patients With Acute Lung Injury[J]. JAMA, 2012, 307(8): 795-803. DOI:10.1001/jama.2012.137 |
| [17] | Arabi YM, Aldawood AS, Haddad SH, et al. Permissive Underfeeding or Standard Enteral Feeding in Critically Ill Adults[J]. N Engl J Med, 2015, 373(12): 1174-1175. DOI:10.1056/NEJMoa1502826 |
| [18] | Rice TW, Mogan S, Hays MA, et al. Randomized trial of initial trophic versus full-energy enteral nutrition in mechanically ventilated patients with acute respiratory failure[J]. Crit Care Med, 2011, 39(5): 967-974. DOI:10.1097/CCM.0b013e31820a905a |
| [19] | Rugeles S, Rueda JD, Díaz CE, et al. Hyperproteic hypocaloric enteral nutrition in the critically ill patient:A randomized controlled clinical trial[J]. Indian J Crit Care Med, 2013, 17(6): 343-9. DOI:10.4103/0972-5229.123438 |
| [20] | 林少华, 燕晓雯, 郭光远, 等. 充分肠内营养与低剂量肠内营养对急性肺损伤患者影响的临床研究[J]. 中华全科医师杂志, 2014, 13(4): 301-304. DOI:10.3760/cma.j.issn.1671-7368.2014.04.020 |
| [21] | Doig GS, Heighes PT, Simpson F, et al. Early enteral nutrition, provided within 24 h of injury or intensive care unit admission, significantly reduces mortality in critically ill patients:a Meta-analysis of randomised controlled trials[J]. Intensive Care Med, 2009, 35(12): 2018-2027. DOI:10.1007/s00134-009-1664-4 |
| [22] | Doig GS, Heighes PT, Simpson F, et al. Early enteral nutrition reduces mortality in trauma patients requiring intensive care:a Meta-analysis of randomised controlled trials[J]. Injury, 2011, 42(1): 50-56. DOI:10.1016/j.injury.2010.06.008 |
| [23] | Mentec H, Dupont H, Bocchetti M, et al. Upper digestive intolerance during enteral nutrition in critically ill patients:frequency, risk factors, and complications[J]. Crit Care Med, 2001, 29(10): 1955-1961. DOI:10.1097/00003246-200110000-00018 |
 2018, Vol. 27
2018, Vol. 27




