晕厥预后从大多数的良性过程到少数患者的猝死,预后相差很大。怎样从众多的晕厥患者中识别出高危患者,给予及时、准确的干预及治疗,可能会对高危晕厥患者的预后产生重大的影响。晕厥的病因涉及多个学科,在急诊科较短的就诊时间内确定晕厥的病因尤为困难。所以在急诊临床工作中,识别高危晕厥患者,给予及时、准确的干预及治疗,减少晕厥患者在急诊科猝死风险,是晕厥诊治过程中重要的环节。回顾性分析2010年6月至2016年6月空军总医院以晕厥为主诉或病程中伴发晕厥共516例的临床资料,希望从中寻找出晕厥患者发生死亡的危险因素,能对急诊临床工作有所帮助。现报道如下。
1 资料与方法 1.1 一般资料 1.1.1 入选病例选择2010年6月至2016年6月期间住院治疗及在急诊科死亡的以晕厥为主诉或病程中伴发晕厥共516例患者的临床资料,其中男性321例(62.2%),女性195例(37.8%);年龄(62.23±19.69)岁。所有病例均经临床诊断及鉴别诊断排除了癫痫发作、低血糖、头部外伤后的短暂意识丧失后入选。
(1)晕厥分类标准标准其中心源性晕厥、神经介导的反射性晕厥、体位性低血压及直立不耐受综合征晕厥分类根据2014年晕厥诊断与治疗中国专家共识[1]及2017年美国ACC/AHA/HRS晕厥诊断与处理指南[2]诊断标准入选;晕厥相关不常见疾病、不明原因的晕厥分类根据2017年美国ACC/AHA/HRS晕厥诊断与处理指南[2]诊断标准入选。
(2)心源性晕厥共入选164例。包括:①急性心肌梗死入选49例,其中37例心电图、肌钙蛋白、冠脉造影符合均符合急性心肌梗死表现。另12例未行冠脉造影检查,但心电图、肌钙蛋白、临床症状可确诊急性心肌梗死,其中4例在急诊科死亡未住院患者,包括1例心电图表现急性下壁心肌梗死并发Ⅲ度房室传导阻滞,肌钙蛋白及CK-MB阳性患者;还包括2例表现为左主干心电图表现且肌钙蛋白及CK-MB阳性患者;另1例心电图表现多导联ST段明显压低且肌钙蛋白及CK-MB阳性患者。②心律失常入选71例,具体如下:Ⅲ度房室传导阻滞10例,其中1例永久起搏器植入术后起搏器功能异常致晕厥;Ⅱ度Ⅱ型房室传导阻滞5例;病窦综合征4例,最长RR间期均≥3 s;房颤合并病窦综合征13例,且此13例最长RR间期均≥3 s;房颤合并Ⅱ度房室传导阻滞6例,且此6例最长RR间期均≥3 s;病窦综合征(Ⅱ度以上窦房传导阻滞)6例, 且且此6例最长RR间期均≥3 s;房扑合并病窦综合征2例,最长RR间期均≥3 s,其中1例RR间期达6.18 s;窦性心律不齐并心动过缓7例,清醒状态下心率均持续 < 40次/min,其中1例肾功能衰竭高血钾致窦性停搏;阵发性室上性心动过速3例,其中2例为预激综合征;快速型房扑1例,心室率达223次/min时晕厥;风湿性心脏病合并快速型房颤1例,心室率达220次/min以上时晕厥;室速9例,其中5例并发室颤,1例尖端扭转型室速,1例长QT间期综合征,另2例晕厥入院,多次发生室速、室颤,1例在急诊科死亡,另1例存活,引起室速及室颤的原因不明;Brugada综合征1例,晕厥时性质不明,后晕厥当天发生猝死;长QT间期综合征1例,入院前晕厥,入院后心电监护未发生新的心律失常;窦性停搏1例,消化道出血致高钾血症引起;1例既往房颤伴病窦综合征植入永久起搏器,入院前晕厥,后入急诊科前数分钟心搏呼吸停止,心肺复苏后,可排除起搏器功能异常、急性冠脉综合征、肺栓塞、主动脉夹层等疾病,考虑恶性心律失常引起晕厥。③4例主动脉瓣重度狭窄患者、1例扩张性心肌病患者、1例肥厚性心肌病患者、1例室间隔缺损患者、3例冠心病、2例高血压性心脏病、1例肺心病、1例肾功能衰竭、1例肿瘤晚期患者共15例,共同表现为喘憋、双下肢凹陷性水肿、肺部细湿啰音、胸片心影扩大、BNP明显增高、心脏超声EF值明显降低。④肺血栓栓塞症23例,其中17例经肺增强CT确诊,1例经肺动脉造影确诊,1例经核素肺灌注确诊;另4例在急诊科死亡患者,其中2例床旁超声发现下肢近心端深静脉血栓,根据2014年欧洲心脏学会急性肺栓塞诊断治疗指南[3]中“临床疑似肺栓塞患者,CUS显示深静脉深静脉近段血栓,则可确诊肺栓塞”的标准,确诊为PTE;另2例WELLS评分均﹥6分,根据Ulukavak[4]及吴本权[5]报道的‘Wells评分大于6分预测PTE符合率达100%’的标准,,且均发生猝死,可诊断为肺血栓栓塞症。⑤主动脉夹层破裂6例,其中5例主动脉增强CT确诊,余1例经超声可见升主动脉内破裂的内膜片漂浮。
(3)神经介导的反射性晕厥共入选205例。包括:①血管迷走性晕厥75例,直立体位引起30例;紧张、疼痛恐惧等情绪引起28例,其他17例经直立倾斜试验诊断。②情境性晕厥118例,其中排尿引起22例,排便引起22例,咳嗽16例,腹痛7例,进食引起30例,运动后10例,其他11例。③颈动脉窦性晕厥5例。④不典型晕厥7例。
(4)体位性低血压及直立不耐受综合征,共入选73例包括:①由体位改变引起33例;②药物引起6例,其中4例服用硝酸甘油引起,1例服用消心痛,1例调整降压药物后引起;酒精引起7例;③血容量不足10例,其中消化道出血引起4例;多次腹泻引起3例;长期进食差2例;1例发热后大量出汗引起;④动态血压诊断8例;卧立位试验及直立倾斜试验时诊断7例;2例帕金森引起原发性自主神经功能衰竭。
(5)晕厥相关不常见疾病。根据2017 ACC/AHA/HRS晕厥诊断与处理指南诊断标准,入选19例,包括:①锁骨下动脉盗血6例;②烟雾病1例;③双侧大脑前动脉闭塞1例、双侧大脑后动脉闭塞1例、左大脑中动脉中度狭窄合并右大脑中动脉重度狭窄1例、左侧颈动脉狭窄58%合并右侧颈动脉狭窄48%1例、双侧大脑后动脉重度狭窄1例、左颈内动脉及左大脑中动脉及左大脑前动脉闭塞1例、左大脑后动脉及右大脑中动脉重度狭窄1例、左侧劲内动脉狭窄60%合并右侧颈内动脉支架内狭窄50%1例④非外伤性蛛网膜下腔出血2例。
(6)不明原因的晕厥。根据2017 ACC/AHA/HRS晕厥诊断与处理指南定义,共入选55例,此55例均有心电图检查(100%);行动态心电图检查39例(70.9%);行动态血压检查21例(38.2%);行颅脑核磁平扫(MRI)49例(89.1%),未行MRI的6例均经颅脑CT检查;行MRA检查36例(65.5%),未行MRA检查者19例中有11例经颅脑TCD检查;行脑电图或动态脑电图检查34例(61.8%);行颈部血管超声检查51例(92.7%);行心脏超声检查50例(90.9%)。以上检查及其他实验室检验及临床症状及体征均不能明确晕厥病因,并且病例资料经多专科医生及急诊科医生共同讨论后确定入选为不明原因的晕厥。
1.2 观察指标及方法由不知研究目的的医生进行患者临床资料采集,资料汇总后由心血管内科、神经内科、神经外科、呼吸内科、急诊科各1名副主任医师共同讨论决定晕厥的分类。
1.3 本研究符合医学伦理学标准所有检测和治疗均获得患者家属的知情同意。
1.4 统计学方法应用SPSS 16.0(SPSS, Chicago, IL, USA)统计软件进行数据处理。所有数据采用Logistic回归分析进行多因素分析。以P < 0.05为差异有统计学意义。
2 结果 2.1 以是否发生死亡为二值因变量以年龄(定量变量,未分组)、性别、既往是否有吸烟史及饮酒史、既往是否有高血压、糖尿病、高脂血症病史,是否心源性晕厥、是否神经介导性晕厥、是否体位性低血压或直立不耐受综合征、是否晕厥相关不常见疾病、是否不明原因性晕厥12个自变量,采用多因素logistic回归分析法筛选自变量,结果性别、既往是否有吸烟史及饮酒史、既往是否有高血压、糖尿病、高脂血症病史、是否神经介导性晕厥、是否晕厥相关不常见疾病性晕厥、是否不明原因性晕厥等9个自变量被筛除了;年龄、是否心源性晕厥、是否体位性低血压或直立不耐受综合征等3个因素在回归方程中有响应。然后再将这3个自变量分别代入回归方程中进行进行分析,结果是否体位性低血压或直立不耐受综合征项无统计学意义(见表 1);年龄项(见表 2)及是否心源性晕厥项(见表 3)有统计学意义。年龄、是否心源性晕厥、是否体位性低血压或直立不耐受综合征等3个因素同时代入回归方程中,这三种因素均有统计学意义,结果见表 4。
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.178 5 | -2.487 4 | 194.211 0 | < 0.01 | ||
| 是否体位性低血压或直立不耐受综合征 | 0.544 4 | -0.360 5 | 0.438 4 | 0.507 9 | 0.697 | 0.240~2.027 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.838 6 | -4.950 6 | 34.853 8 | < 0.01 | ||
| 年龄 | 0.011 5 | 0.035 9 | 9.803 9 | 0.001 7 | 1.037 | 1.014~1.060 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.381 8 | -3.897 6 | 104.227 6 | < 0.01 | ||
| 是否心源性晕厥 | 0.430 7 | 2.441 2 | 32.122 7 | < 0.01 | 11.487 | 4.938~26.721 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 1.051 2 | -6.666 5 | 40.221 4 | < 0.01 | ||
| 年龄 | 0.012 4 | 0.032 4 | 6.862 4 | 0.008 8 | 1.033 | 1.008~1.058 |
| 是否心源性晕厥 | 0.615 8 | 2.980 8 | 23.432 6 | < 0.01 | 19.704 | 5.894~65.875 |
| 是否体位性低血压或直立不耐受综合征 | 0.779 5 | 1.668 4 | 4.581 2 | 0.032 3 | 5.304 | 1.151~24.441 |
以年龄(定量变量,未分组)、性别、既往是否有吸烟史及饮酒史、既往是否有高血压、糖尿病、高脂血症病史,是否心源性晕厥、是否神经介导性晕厥、是否体位性低血压或直立不耐受综合征、是否晕厥相关不常见疾病、是否不明原因性晕厥等因素及以上因素两两交互作用产生新的派生变量为自变量,采用前进法、后退法、逐步回归分析法筛选自变量,结果是否心源性晕厥项及年龄与年龄、年龄与是否心源性、是否高血压与是否体位性低血压与直立不耐受综合征、有无饮酒史与是否神经介导性晕厥等派生变量在回归方程中有响应。再将这五个变量分别代入回归方程,结果既往有无饮酒史与是否神经介导性晕厥交互作用派生项(表 5)、是否高血压与是否体位性低血压与直立不耐受综合征交互作用派生项(表 6)无统计学意义(P均 > 0.05);年龄与年龄交互作用派生项(表 7)、是否心源性晕厥项(表 8)、年龄与是否心源性晕厥交互作用派生项(表 9)有统计学意义(P均 < 0.05)。然后将这5种因素同时代入回归方程时,这五种因素项均有统计学意义(P均 < 0.05),结果见表 10。
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.170 9 | -2.518 1 | 217.115 0 | < 0.01 | ||
| 既往有无饮酒史与是否神经介导性晕厥 | 1.040 1 | -0.426 3 | 0.168 0 | 0.681 9 | 0.653 | 0.085~5.014 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.177 9 | -2.578 4 | 210.097 8 | < 0.01 | ||
| 是否高血压与是否体位性低血压与直立不耐受综合征 | 0.561 2 | 0.563 5 | 1.008 3 | 0.315 3 | 1.757 | 0.585~5.278 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.490 1 | -3.919 3 | 63.958 7 | < 0.01 | ||
| 年龄与年龄 | 0.000 086 | 0.000 287 | 11.2119 | 0.000 8 | 1.000 | 1.000~1.000 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.381 8 | -3.897 6 | 104.227 6 | < 0.01 | ||
| 是否心源性晕厥 | 0.430 7 | 2.441 2 | 32.122 7 | < 0.01 | 11.487 | 4.938~26.721 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 0.335 0 | -3.731 0 | 124.014 1 | < 0.01 | ||
| 年龄与是否心源性晕厥 | 0.005 34 | 0.032 4 | 36.666 5 | < 0.01 | 1.033 | 1.022~1.044 |
| 危险因素 | SE | β值 | χ2值 | P值 | OR值 | 95%CI |
| Intercept | 1.910 6 | -9.171 7 | 23.044 4 | < 0.01 | ||
| 有无饮酒史与是否神经介导性晕厥 | 1.402 8 | 3.257 6 | 5.392 7 | 0.020 2 | 25.987 | 1.662~406.268 |
| 是否高血压与是否体位性低血压与直立不耐受综合征 | 0.926 4 | 2.315 7 | 6.248 8 | 0.012 4 | 10.132 | 1.649~62.263 |
| 年龄与年龄 | 0.000 264 | 0.000 751 | 8.069 0 | 0.004 5 | 1.001 | 1.000~1.000 |
| 是否心源性晕厥 | 2.744 2 | 8.937 2 | 10.606 7 | 0.001 1 | > 999.999 | 35.118~999.999 |
| 年龄与是否心源性晕厥 | 0.032 4 | -0.072 1 | 4.960 0 | 0.025 9 | 0.930 | 0.873~0.991 |
|
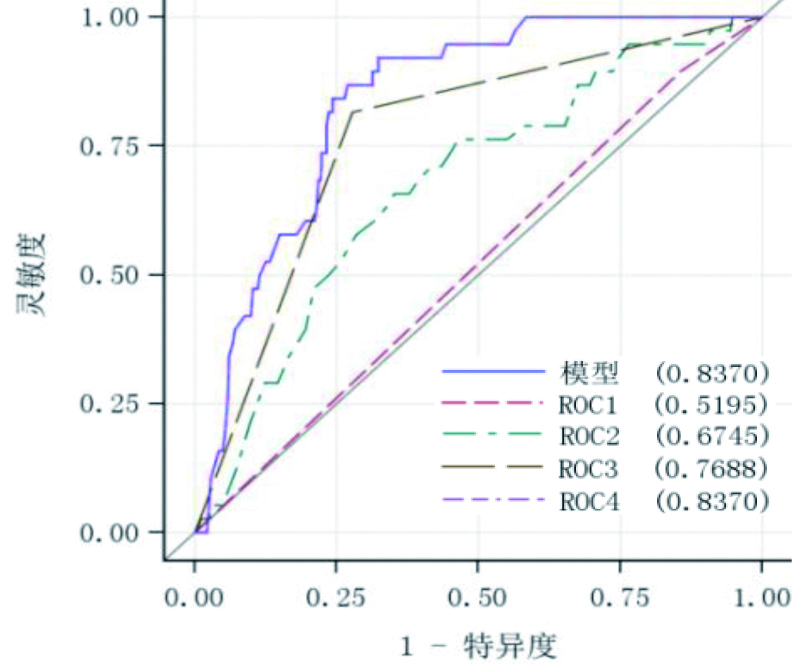
| ROC1:是否体位性低血压或直立不耐受综合征项;ROC2:年龄项;ROC3:是否心源性晕厥项;ROC4:三种因素共同参与 图 1 未加入派生变量的ROC曲线图比较 Figure 1 Comparison of ROC curves without derivative variables |
|
|
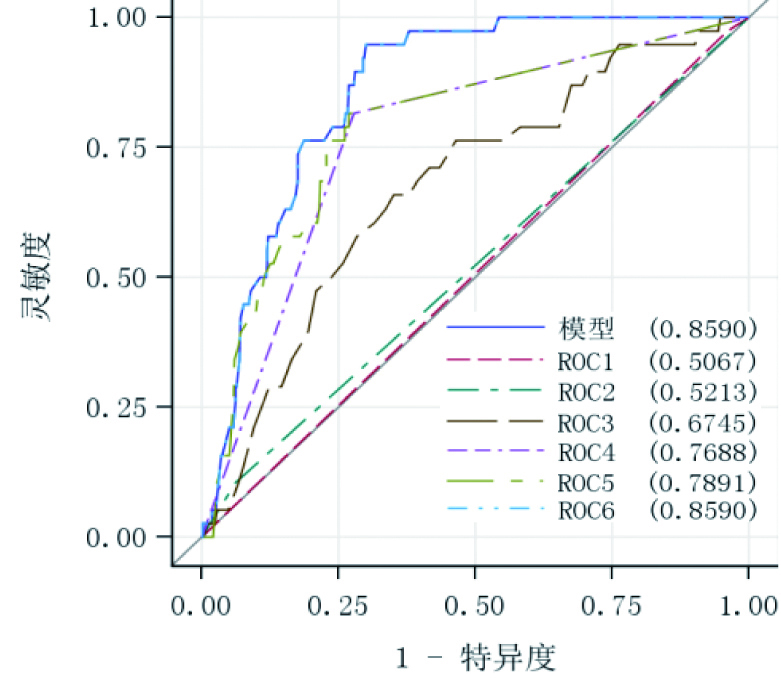
模型的ROC曲线下面积0.8370,说明此回归方程预测死亡的准确率较高。是否心源性晕厥项的ROC曲线下面积0.7688,年龄项ROC曲线下面积0.6745。ROC关联统计量见表 11。将回归方程模型ROC曲线、五个变量共同代入回归方程的ROC曲线以及这五个变量分别代入回归方程的ROC曲线汇总比较(图 2),此回归方程的ROC曲线下面积0.8590,说明此方程对预测是否发生死亡的准确率较高;心源性晕厥项ROC曲线下面积0.7688,年龄与年龄交互作用派生项ROC曲线下面, 0.6745,年龄与是否心源性晕厥交互作用派生项ROC曲线下面, 0.7891,说明这三种危险因素对预测晕厥患者是否死亡的准确率相对较高。ROC关联统计量见表 12。
|
| ROC1:既往有无饮酒史与是否神经介导性晕厥项; ROC2:是否高血压与是否体位性低血压与直立不耐受综合征; ROC3:年龄与年龄项; ROC4:是否心源性晕厥项; ROC5:年龄与是否心源性晕厥项ROC6:五种因素共同参与项 图 2 加入派生变量的ROC曲线图比较 Figure 2 Comparison of ROC curves with derivative variables |
|
|
| ROC模型 | Mann-Whitney | Somers'D(Gini) | Gamma | Tau-a | ||
| 面积 | SE | 95%CI | ||||
| 模型 | 0.837 0 | 0.025 5 | 0.786 9~0.887 0 | 0.673 9 | 0.677 6 | 0.092 1 |
| ROC1(是否体位性低血压或直立不耐受综合征项) | 0.519 5 | 0.026 5 | 0.467 6~0.571 4 | 0.039 1 | 0.178 3 | 0.005 34 |
| ROC2(年龄项) | 0.674 5 | 0.044 4 | 0.587 5~0.761 6 | 0.349 1 | 0.355 4 | 0.047 7 |
| ROC3(是否心源性晕厥项) | 0.768 8 | 0.033 5 | 0.703 2~0.834 4 | 0.537 5 | 0.839 8 | 0.073 5 |
| ROC4(三种因素共同参与) | 0.837 0 | 0.025 5 | 0.786 9~0.887 0 | 0.673 9 | 0.677 6 | 0.092 1 |
| ROC模型 | Mann-Whitney | Somers'D(Gini) | Gamma | Tau-a | ||
| 面积 | SE | 95%CI | ||||
| 模型 | 0.859 0 | 0.022 0 | 0.861 0~0.902 1 | 0.718 1 | 0.721 6 | 0.098 2 |
| ROC1(既往有无饮酒史与是否神经介导性晕厥) | 0.506 7 | 0.013 9 | 0.479 5~0.534 0 | 0.013 4 | 0.210 0 | 0.001 84 |
| ROC2(是否高血压与是否体位性低血压与直立不耐受综合征) | 0.521 3 | 0.025 8 | 0.470 6~0.571 9 | 0.042 5 | 0.274 5 | 0.005 81 |
| ROC3(年龄与年龄) | 0.674 5 | 0.044 4 | 0.587 5~0.761 6 | 0.349 1 | 0.355 4 | 0.047 7 |
| ROC4(是否心源性晕厥) | 0.768 8 | 0.033 5 | 0.703 2~0.834 4 | 0.537 5 | 0.839 8 | 0.073 5 |
| ROC5(年龄与是否心源性晕厥) | 0.789 1 | 0.037 0 | 0.716 6~0.861 5 | 0.578 1 | 0.670 1 | 0.079 0 |
| ROC6(五种因素共同参与) | 0.859 0 | 0.022 0 | 0.816 0~0.902 1 | 0.718 1 | 0.721 6 | 0.098 2 |
多因素logistic回归分析结果显示:年龄及是否心源性晕厥是晕厥患者30天内死亡的独立危险因素。再将以上因素两两交互作用产生新的派生因素进行多因素分析,是否心源性晕厥项、年龄与年龄交互作用派生项、年龄与是否心源性晕厥交互作用派生项是晕厥患者30天内死亡的独立危险因素。国外研究[6]年龄 > 60岁是晕厥患者的短期(≤30 d)危险因素,本研究结果无论是否加入派生因素,年龄均与晕厥的预后密切相关,与上述研究结果一致。本研究亦显示无论是否加入派生变量,是否心源性晕厥都是晕厥患者的短期(≤30 d)发生死亡的独立危险因素。2017年美国ACC/AHA/HRS晕厥诊断与处理指南指出,心源性晕厥比神经介导性晕厥预后差[2]。更多的研究显示:结构性心脏病[6~10]、心力衰竭[6, 7, 11, 12]、心源性猝死家族史[8]、异常心电图[11, 13~16]、肌钙蛋白阳性[16]等因素是晕厥患者的短期(≤30 d)危险因素。本研究与以上研究结果一致。在派生因素中,年龄与年龄交互产生的派生变量、年龄与是否心源性晕厥交互作用产生的派生变量是晕厥患者发生死亡的短期(≤30 d)危险因素,这更说明年龄与是否心源性晕厥与晕厥患者的预后紧密相关。
回顾分析本研究共入选死亡病例38例。神经介导性晕厥死亡3例,其中1例肿瘤晚期衰竭患者,多次进食时晕厥,后死于肺部感染及多脏器功能衰竭;另1例入院前7 d排尿时晕厥,入院后经各项检查排除心源性晕厥,入院后第8天新发心肌梗死死亡;第3例排便时晕厥,致伤头部,颅内出血死亡。体位性低血压或直立不耐受综合征死亡4例,1例胰腺癌晚期,长期腹泻,容量不足致体位性低血压多次晕厥,后死于肺部感染及多脏器功能衰竭;另1例进食明显减少半月余,容量不足致体位性低血压性晕厥入院,后死于肺部感染;另1例严重贫血,肾功能衰竭长期透析患者,体位性低血压入院,后死于肺部感染;另1例肿瘤晚期,入院前肺部感染致进食差,体位性低血压晕厥,后死于肺部感染。以上患者死亡时间均在入院后7天以后。心源性晕厥死亡31例,其中急性心肌梗死13例;心律失常5例;各种器质性心脏病致心力衰竭死亡5例;急性肺血栓栓塞症死亡5例;主动脉夹层死亡3例。并且心源性晕厥死亡的患者,有16例在急诊科死亡。将心源性晕厥死亡患者与非心源性晕厥死亡患者特点进行比较发现:①心源性晕厥死亡患者发生晕厥与死亡的直接病因是一致的,而非心源性晕厥患者发生晕厥的直接病因不一致。②心源性晕厥患者发病急,容易在急诊科死亡,需要争分夺秒明确病因。③在治疗或去除引起晕厥的直接病因后,在心源性晕厥患者来讲,可能会预后不同[17];而非心源性晕厥患者,积极治疗或去除引起晕厥的直接病因后,对患者的预后影响不大。这说明急诊科对晕厥患者的积极、正确的诊治策略及临床路径,可能会影响整体晕厥患者的预后,是晕厥诊治的基础和非常重要的环节。而2017年美国ACC/AHA/HRS联合急诊医学会共同发布晕厥指南,也侧面说明急诊科在晕厥诊治中的重要地位。
而据山东大学齐鲁医院急诊科[18]报道,2004年-2014年10年间,猝死和心、脑血管疾病占到急诊死亡的前三位,且猝死患者所占比例逐年升高,2014年占21.1%,居急诊死亡病因第一位。这提示猝死及心血管疾病是目前急诊科面临的一个重要问题。而心源性晕厥患者发生死亡的方式往往表现为猝死,并且有些心源性晕厥病因比较隐蔽,增加了诊断的难度。而有时晕厥症状以及晕厥引起的外伤有可能影响或延误是否心源性晕厥的诊断。例如1例晕厥患者致伤头部,D-二聚体轻度升高考虑是否外伤引起,行颅脑CT后回抢救室后猝死,后抢救时行床旁超声检查单侧下肢深静脉血栓形成,右心室扩大,肺动脉高压,考虑肺血栓栓塞症,后抢救无效死亡。另1例晕厥2次入急诊科,伴胸痛,入科后5 min再次晕厥,清醒后一侧肢体偏瘫,是否神经系统疾病导致的晕厥?是否该快速行颅脑CT明确急性脑血管病的诊断?而笔者选择急诊床旁超声,发现主动脉夹层破裂,主动脉内漂浮的内膜片堵塞了一侧颈动脉导致患者出现偏瘫。另外分析本研究中入选病例发现虽然行颅脑CT及颅脑核磁共振扫描(未增强)检查患者较多,可发现晕厥病因的阳性率较低,这与2017年美国ACC/AHA/HRS晕厥诊断与处理指南[2]结论一致。通过以上结果的分析,似乎急诊科医生应对晕厥的思路逐渐清晰:接诊晕厥患者后,首先应优先心源性晕厥的诊断及鉴别诊断;若可疑心源性晕厥,则优先考虑或排除急性心肌梗死、恶性心律失常、器质性心脏病致心力衰竭、肺栓塞、主动脉夹层,因为这五种疾病伴发晕厥患者可能在急诊科很快发生猝死。
| [1] | 刘文玲, 胡大一, 郭继鸿, 等. 晕厥诊断与治疗中国专家共识(2014年更新版)[J]. 中华内科杂志, 2014, 53(11): 916-925. DOI:10.3760/cma.j.issn.0578-1426.2014.11.022 |
| [2] | Konstantinides SV, Torbicki A, Perrier A, et al. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism[J]. Eur Heart J, 2014, 35(43): 3033-3073. DOI:10.1093/eurheartj/ehu283 |
| [3] | Ulukavak CT, KÖktÜrkN, Demir N, et al. Comparison of three clinical prediction rules among patients with suspected pulmonary embolism[J]. Tuberktoraks, 2005, 53(3): 252-258. |
| [4] | 吴本权, 张文先, 刘慧, 等. Wells量表和修正的Geneva评分对肺栓塞的预测价值[J]. 中山大学学报(医学科学版), 2009, 30(4): 477-481. DOI:10.3321/j.issn.1672-3554.2009.04.026 |
| [5] | Shen W-K, Sheldon RS, Benditt DG, et al. 2017 ACC/AHA/HRS guideline for the evaluation and management of patients with syncope: a report of the American College of Cardiology /American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society[J]. J Am Coll Cardiol, 2017, 70(5): e39-110. DOI:10.1016/j.jacc.2017.03.003 |
| [6] | Gabayan GZ, Derose SF, Asch SM, et al. Predictorsof short-term (seven-day) cardiaoutcomes afteremergency department visit for syncope[J]. Am J Cardiol, 2010, 105(11): 82-86. DOI:10.1016/j.amjcard.2009.08.654 |
| [7] | D'Ascenzo F, Biondi-Zoccai G, Reed MJ, et al. Incidence, etiology and predictors of adverse outcomes in 43, 315 patients presenting to the emergency department with syncope: an international metaanalysis Int[J]. J Cardiol, 2013, 167(1): 57-62. DOI:10.1016/j.ijcard.2011.11.083 |
| [8] | Grossman SA, Fischer C, Lipsitz LA, et al. Predicting adverse outcomes in syncope[J]. J Emerg Med, 2007, 33(13): 233-239. DOI:10.1016/j.jemermed.2007.04.001 |
| [9] | Grossman SA, Babineau M, Burke L, et al. Applying the Boston syncope criteria to near syncope[J]. J Emerg Med, 2012, 43(6): 958-963. DOI:10.1016/j.jemermed.2012.01.043 |
| [10] | Numeroso F, Mossini G, Lippi G, et al. Evaluation of the current prognostic role of heart diseases in the history of patients with syncope[J]. Europace, 2014, 16(19): 1379-1383. DOI:10.1093/europace/eut402 |
| [11] | Sarasin FP, Hanusa BH, Perneger T, et al. A risk score to predict arrhythmias in patients with unexplained syncope[J]. Acad Emerg Med, 2003, 10(12): 1312-1317. DOI:10.1197/S1069-6563(03)00535-9 |
| [12] | Derose SF, Gabayan GZ, Chiu VY, et al. Patterns and preexisting risk factors of 30-day mortality after a primary discharge diagnosis of syncope or near syncope[J]. Acad Emerg Med, 2012, 19(15): 488-496. |
| [13] | Quinn JV, Stiell IG, McDermott DA, et al. Derivation of the San Francisco Syncope Rule to predict patients with short-term serious outcomes[J]. Ann Emerg Med, 2004, 43(2): 224-232. DOI:10.1016/S0196-0644(03)00823-0 |
| [14] | Costantino G, Perego F, Dipaola F, et al. Short- and long-term prognosis of syncope, risk factors, and role of hospital admission: results from the STePS (Short-Term Prognosis of Syncope) study[J]. J Am Coll Cardiol, 2008, 51(3): 276-283. DOI:10.1016/j.jacc.2007.08.059 |
| [15] | Daccarett M, Jetter TL, Wasmund SL, et al. Syncope in the emergency department: comparison of standardized admission criteria with clinical practice[J]. Europace, 2011, 13(11): 1632-1638. DOI:10.1093/europace/eur201 |
| [16] | Sun BC, Derose SF, Liang LJ, et al. Predictors of 30-day serious events in older patients with syncope[J]. Ann Emerg Med, 2009, 54(16): 769-778. DOI:10.1016/j.annemergmed.2009.07.027 |
| [17] | 石桂良, 邓新桃, 郑金国, 等. 经皮冠状动脉介入治疗冠心病晕厥的疗效观察[J]. 中华急诊医学杂志, 2013, 22(6): 651-653. DOI:10.3760/cma.j.issn.1671-0282.06.026 |
| [18] | 程凯, 张略韬, 徐峰, 等. 山东省某三甲医院2004—2014年急诊患者病死率研究[J]. 中华急诊医学杂志, 2016, 25(7): 927-931. DOI:10.3760/cma.j.issn.1671-0282.2016.07.017 |
 2018, Vol. 27
2018, Vol. 27




