经鼻高流量吸氧(high-flow nasal cannula, HFNC)装置是对传统吸氧装置的革新,它的最大吸气流速可达到40~60 L/min,在37℃下可达到100%湿化效果,患者闭嘴呼吸时拥有呼吸末正压效应(PEEP效应)[1-2]。HFNC系统因其独特的生理学效应,越来越多的医护人员应用它来预防或者治疗拔管后呼吸衰竭的患者,拔管后应用高流量氧疗可以减少拔管后呼吸衰竭的发生和降低再插管率[3-4],其使用效果不亚于无创呼吸机的效果;但目前临床上对于HFNC在脱机拔管后应用的适宜人群仍不明确,仍需临床研究进一步证实。
肺部超声评分(lung ultrasound score, LUS)是通过床旁超声评估肺部通气情况的一种方法,是急诊危重症超声的重要组成部分之一,在急诊及ICU广泛应用已超过10年;该超声评估手段已经被证实可以预测ARDS的发生,机械通气患者的拔管失败率以及急性呼吸衰竭患者的插管率[5]。已有多项国外多中心研究证实肺部超声评分通过准确评估机械通气患者拔管前,拔管后的肺通气情况来预测拔管后的再插管率的风险值;LUS≥14分的ICU患者拔管后的发生呼吸衰竭及再插管率明显高于LUS<14分的患者[6-7]。
本研究首次通过肺部超声评分筛选出拔管后出现呼吸衰竭高风险的患者,通过使用HFNC治疗与普通氧疗(鼻导管或面罩吸氧)比较,验证前者是否可以降低这类高风险患者的再插管率,并减少ICU住院时间、改善患者的呼吸、循环及氧合情况;探讨HFNC在此类高风险拔管患者中是否较其他低风险拔管患者有更加明显的作用,现分析总结如下。
1 资料与方法 1.1 一般资料 1.1.1 研究类型及伦理问题本研究为单中心随机对照前瞻性研究,入组患者使用RedCap系统进行随机分组并录入数据。本研究符合医学伦理学标准,在获得医院伦理委员会批准同意后使用患者资料进行科学分析[审批号:2015伦审研067号(浙医二院)],并获得患者或家属的知情同意。
1.1.2 研究对象选取2016年5月至2017年5月收入一家大学附属的三级甲等综合性医院(浙江大学医学院附属第二医院)急诊ICU并行机械通气患者,符合脱机拔管标准及入组标准,拔管前行肺部超声评分(LUS)≥14分。
1.1.3 入组标准⑴年龄大于18岁
⑵患者气管插管行机械通气治疗时间≥48 h
⑶脱机前实验成功:呼吸机压力支持≤10 cmH2O(1cmH2O=0.098Kpa);FiO2 ≤ 50%;SpO2 ≥ 95%及呼吸频率≤25次/min;呼出潮气量>7 mL/kg,漏气实验阳性,48 h内没有择期手术的安排;
⑷脱机前GCS评分≥10分;
⑸T<38.5℃;
⑹去甲肾上腺素使用量<0.2μg/(kg·min),收缩压>90 mmHg(1 mmHg=0.133Kpa)并且没有低血压的临床表现;
⑺家属签署知情同意书。
1.1.4 排除标准⑴需行气管切开患者;
⑵颈8椎体平面以上损伤并伴有截瘫症状;
⑶确诊或疑似气胸,胸部手术后;
⑷拒绝签署同意书或放弃治疗患者;
⑸因肥胖,胸廓畸形等原因无法行肺部超声患者。
1.2 研究方法 1.2.1 肺部超声评分方法(1) 符合入组患者由经过专业超声技能培训的急诊ICU主治医师进行肺部超声评估,使用机型为:迈瑞M9超声机(深圳迈瑞公司,中国),使用2-4-MHz腹部超声探头;超声评估时间在患者进行脱机实验成功后,直接录入患者病例资料中。
(2) 评分方案如下[5]:
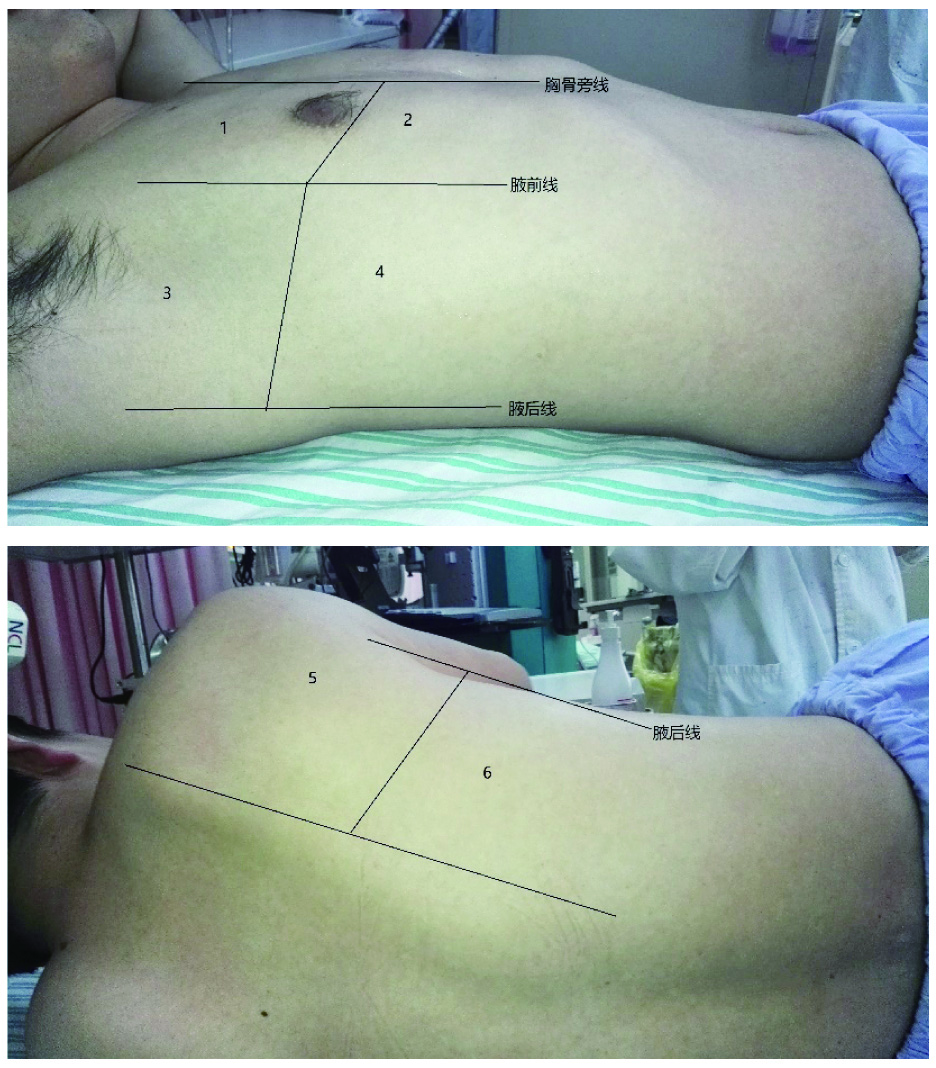
两侧胸部分为2个区域(图 1),每个区域评分为0~3分,总分为36分,评分越高提示肺通气情况越差:0分=正常肺滑动,可见A线或少于3条B线,1分=肺间质综合征(大于三条单一的B线),2分=肺部综合征(融合的B线或白肺),3分=肺实变
|
| 图 1 肺部超声评分示意图:(每侧胸部6各区域,共12区域,总36分) Figure 1 Diagram of the lung ultrasound score (12 regions, calculated as the sum of points ranging from 0 to 36) |
|
|
每日由主管医师评估患者,脱机实验成功后行肺部超声评分,拔管前行肺部超声评分(LUS)≥14分患者入组,使用RedCap系统进行随机分组并录入数据。
⑴干预组(HFNC组):入组后随机分组为干预组患者,拔管后开始使用经鼻导管湿化高流量吸氧装置(HFNC)进行吸氧治疗,HFNC型号(AIRVO2, Optiflow, Fisher & Paykel, Auckland, NewZealand);参数设置为吸入氧体积分数为50%,流量为60 L/min,根据患者氧饱和度调节参数,维持SPO2在93%以上, 持续治疗时间48 h,治疗时间超过48 h后可转为普通吸氧治疗。
⑵对照组[普通氧疗组(conventional oxygen therapy,COT)组]:脱机拔管成功后使用鼻导管或普通面罩吸氧(文丘里或储氧面罩)进行呼吸治疗,参数设置氧流量5 L/min,根据患者氧饱和度调节参数,维持SPO2在93%以上,持续治疗48 h。
1.2.3 入组患者监测随访指标记录入组的两组患者性别、年龄、体质量指数(BMI指数)、连续脏器衰竭评估(SOFA评分)、拔管前机械通气时间、原发疾病等一般资料;入组患者在拔管后6、24及48 h记录心率,呼吸频率及氧饱和度,抽取血气分析并记录相应结果;若患者在48 h内出现呼吸衰竭或拔管失败临床表现,患者将进行重新插管,机械通气治疗。随访记录两组患者ICU住院时间,对于有病情变化,重新插管的患者按同样标准记录以上信息。以上信息均有专业人员及时录入电脑系统中。
1.3 统计学方法应用SigmaStat 3.5 (Systat Software Inc, Point Richmond, CA, USA)软件进行统计学分析。先对计量资料进行正态性检验,符合正态分布的计量资料以均数±标准差(x±s)表示,组间比较采用成组t检验,非正态分布采用Friedman秩和检验;重复测量数据采用重复测量资料的方差分析方法。计数资料以频数和百分数表示,组间比较采用χ2检验;以P<0.05为差异有统计学意义。
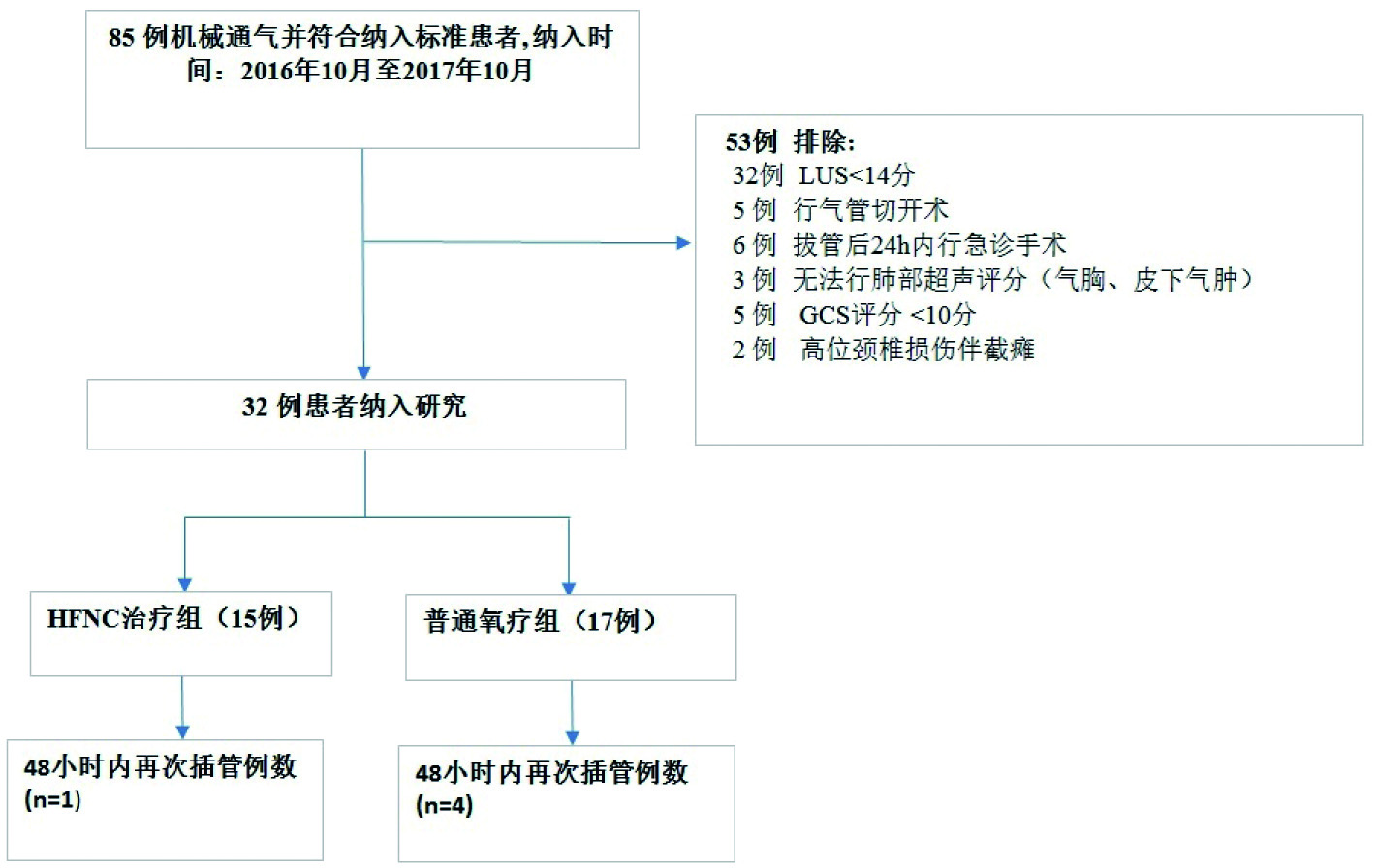
2 结果 2.1 患者入组情况及一般资料入组流程图见图 2:研究期间共入组85例患者,53例患者排除:32例肺部超声评分小于14分,5例行气管切开,6例患者拔管后24 h内行急诊手术,3例因肥胖、或皮下气肿等原因无法行肺部超声,5例患者GCS评分<10分,2例患者为高位颈髓损伤伴截瘫;最终纳入资料完整且符合观察要求的患者32例,其中经鼻高流量氧疗组(HFNC组)15例,常规吸氧治疗组(COT组)17例。一般资料见表 1:两组患者性别、年龄、身体质量指数(BMI指数)、SOFA评分、拔管前机械通气时间、原发疾病等一般资料比较差异无统计学意义(P>0.05)。
|
| 图 2 患者入组流程图 Figure 2 Flowchart of the including patients |
|
|
| 组别 | HFNC组 (n=15) |
COT组 (n=17) |
P值 |
| 年龄(岁) | 38±18 | 45±18 | 0.29 |
| 性别(男/女) | 9/6 | 10/7 | 0.63 |
| BMI | 22±4.1 | 24±4.5 | 0.23 |
| SOFA评分 | 6.1±2.6 | 6.7±2.7 | 0.24 |
| 拔管前机械通气时间(d) | 6.9±2.3 | 6.8±3.5 | 0.96 |
| 再次插管率(例) (%) | 1(6.7%) | 4(23.5%) | <0.01 |
| ICU住院时间(d) | 8.0±2.4 | 10.9±3.5 | <0.01 |
| 原发疾病(例) | |||
| 严重多发伤(无连枷胸) | 6 | 8 | 0.74 |
| 重症肺炎 | 3 | 2 | 0.75 |
| AECOPD | 2 | 1 | 0.63 |
| 腹部外科术后 | 3 | 4 | 0.73 |
| 其他 | 1 | 2 | 0.53 |
| 注:BMI:身体质量指数SOFA评分:连续脏器衰竭评估AECOPD:慢性阻塞性肺气肿急性发作; HFNC:经鼻高流量氧疗COT:普通氧疗 | |||
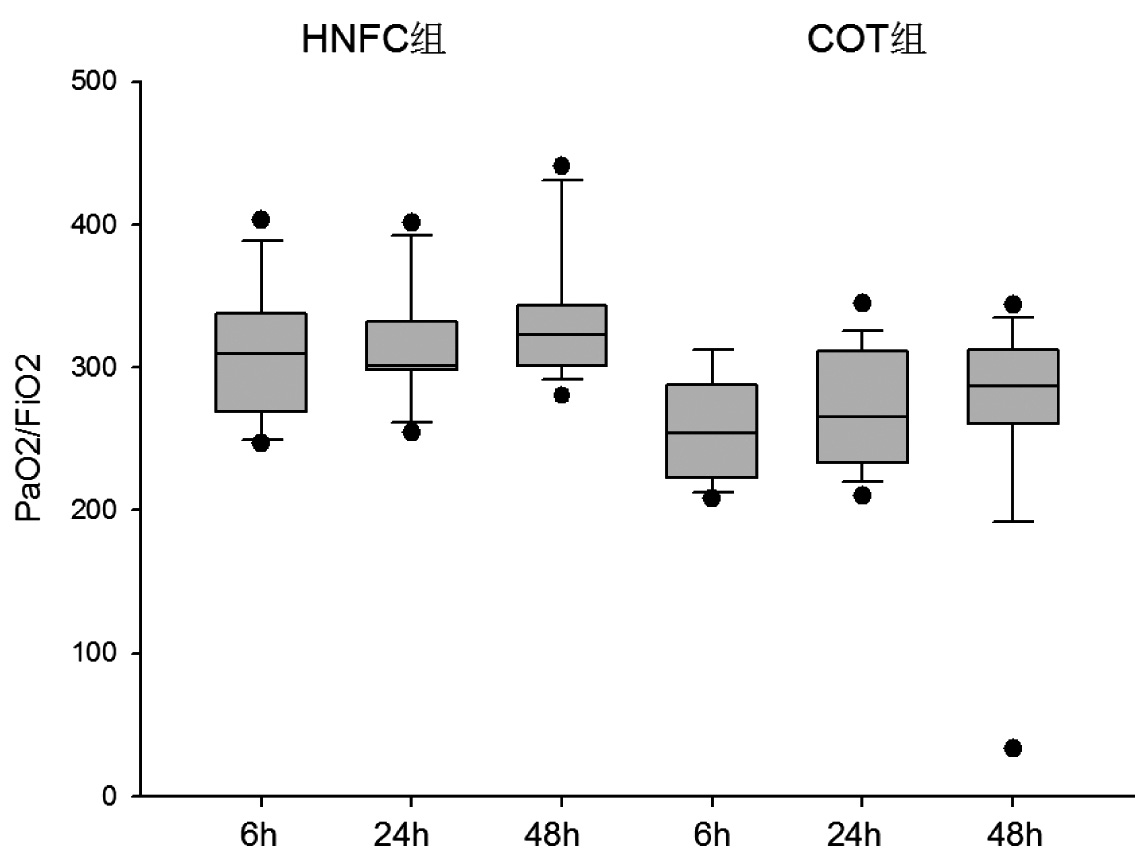
脱机拔管后患者循环及呼吸参数见表 2:脱机拔管后6 h HFNC组患者呼吸频率、心率、氧饱和度(SaO2)、氧合指数(PaO2/FiO2)均优于COT组(P<0.05),患者血气分析中二氧化碳分压(PaCO2)两组差异无统计学意义(P=0.39);脱机拔管后24 h、48 h HFNC组SaO2、PaO2/FiO2均优于COT组(P<0.05),呼吸频率、心率及PaCO2两组差异无统计学意义。图 2可见HFNC组患者氧合指数在各时间点均优于COT组。
| HFNC组(n=15) | COT组(n=17) | P值 | |
| 拔管后6 h | |||
| 呼吸频率(次/min) | 15.8±2.5 | 17.6±2.2 | <0.05 |
| 心率(次/min) | 101±12 | 111±14 | <0.01 |
| SaO2 | 97.8±1.7 | 94.0±2.6 | <0.01 |
| PaO2/FiO2 | 310.1±44.9 | 255.8±35.6 | <0.01 |
| PaCO2(mmHg) | 41.4±7.8 | 45.2±12.1 | 0.39 |
| 拔管后24 h | |||
| 呼吸频率(次/min) | 15.6±1.5 | 16.7±2.2 | 0.11 |
| 心率(次/min) | 91±14.7 | 101±14.1 | 0.058 |
| SaO2 | 97.8±2.2 | 95.2±2.5 | <0.01 |
| PaO2/FiO2 | 314±39.4 | 270.1±41.1 | <0.01 |
| PaCO2(mmHg) | 40±5.3 | 39.9±9.9 | 0.96 |
| 拔管后48 h | |||
| 呼吸频率(次/min) | 15.0±1.7 | 16.1±2.5 | 0.15 |
| 心率(次/min) | 87.7±12.4 | 91.6±12.8 | 0.402 |
| SaO2 | 98.2±2.0 | 97.1±2.2 | <0.05 |
| PaO2/FiO2 | 332.6±43.1 | 273.2±16.2 | <0.01 |
| PaCO2(mmHg) | 35.4±9.7 | 37.7±10.1 | 0.14 |
|
| 图 3 两组患者各时间点氧合指数比较 Figure 3 Comparison of PaO2/FiO2 ratio in two groups |
|
|
HNFC组中拔管后48 h内有1例患者重新插管(6.7%),COT组有4例患者重新插管(23.5%),两组再插管率比较有统计学意义(P<0.01);两组患者ICU住院时间比较:(8.0±2.4) d vs. (10.9±3.5)d,差异有统计学意义(P<0.01)。
3 讨论临床医师在治疗呼吸衰竭患者使用机械通气的过程往往带来许多的并发症,例如呼吸机相关性肺炎(VAP),呼吸机相关性肺损伤(VLI),深静脉血栓(DVT)的形成并导致的肺栓塞,脑梗死等;并且随着机械通气时间的延长,患者出现并发症的几率越大,从而影响患者的预后,并大大的增加了住院费用。许多临床研究已经证实目前ICU中20%~30%的拔管患者在拔管后48 h内会出现呼吸衰竭,这大部分是由于患者通气不足或者是气道的问题导致的[8-9]。拔管出现呼吸衰竭后患者一般需要进行无创呼吸机通气或者重新插管行机械通气。国外相关研究证明拔管后出现呼吸衰竭而再次插管会使患者病死率升高20%~25%左右,并明显延长ICU的住院时间及增加住院费用[10-11]。
随着HFNC的普及,越来越多的医护人员使用它来预防或治疗拔管后的呼吸衰竭。Maggiore等[12]的一个随机对照多中心研究中,105例患者拔管后随机接受文丘里面罩吸氧或HFNC,这些患者包括肺炎、创伤等引起的呼吸衰竭患者。结果显示,HFNC组患者的呼吸频率、氧合指数、舒适度等情况都优于文丘里面罩吸氧组,且差异有统计学意义;HFNC组患者的再插管率明显降低(P=0.01)。Parke等[13]对心脏外科术后患者拔管后使用HFNC与普通氧疗进行比较,高流量氧疗在拔管成功率上有明显优势。但Corley等[14]在心脏外科术后患者(BMI≥30)拔管后使用HFNC与普通氧疗作比较,在拔管成功率、肺不张发生率、呼吸频率及氧合水平上差异无统计学意义。
近年来肺部超声以其床旁、快速、可重复性强、少或无辐射并可应用于特殊人群(儿童、孕妇、肾损伤患者)等优点已广泛应用于急危重症的诊治过程中[15]。Bouhemad等[6]研究显示,在抗生素治疗VAP过程中,肺部超声显示肺部通气改变比床旁X线胸片更为精确。许多研究已证实肺部超声在多种肺部疾病诊断方面具有较强的优势:准确评估俯卧位通气肺部通气变化、呼吸末正压(PEEP)对ARDS的肺复张效果、呼吸相关性肺炎治疗过程中肺通气变化及肺水肿患者肺复张的通气变化[16-20]。Soummer等[7]最早提出并将该方法成功应用于评估脱机拔管后患者肺部通气情况的变化,并证实LUS大于14分患者脱机拔管后再插管率明显增加。
本实验利用肺部超声评分筛选出高风险脱机拔管患者,证明与常规氧疗比较(普通鼻导管或普通面罩吸氧),使用经鼻高流量氧疗可以降低此类患者48 h内的再插管率(6.7% vs. 23.5%);Hernández等[21]对脱机拔管后的低分险患者(低分险患者定义为:年龄小于65岁,拔管当日的急性生理学及慢性健康状况评分<12分,系统体质量指数<30,既往无心肺疾病等标准)72 h内HFNC与常规氧疗组的再插管率进行分析,结果为(8.3% vs. 14.4%);与上述实验相比,本实验HFNC组的再插管率较常规氧疗组的再插管率降低更为明显,证实在肺部超声评估的高风险患者中,HFNC的临床效果和价值可能更加明显。而在Hernández等[22]的另一项对脱机后临床评价为高分险患者(定义为:年龄大于65岁;因为心衰而行机械通气;中到重度的COPD;拔管当日APACHEⅡ评分大于12分;体质量指数大于30;气道完整性问题(包括喉头水肿高风险);清除气道分泌物能力不足;机械通气时间超过7 d)72 h HFNC与无创呼吸机组的再插管率分析结果为(22.8% vs. 19.1%),证实HFNC的效果与无创呼吸机相似,但前者拥有更好的舒适度和患者耐受性。另外,本实验中HFNC对脱机后患者6 h的心率、呼吸频率及氧合指数等指标较COT组有明显改善,可能提示在本实验定义的高风险患者中使用HFNC可以明显改善早期(6 h内)患者脱机拔管后的呼吸窘迫状态,对于脱机拔管后短时间内即出现呼吸衰竭或呼吸窘迫患者效果更为显著,但仍需进一步研究证实,
总之,本研究使用肺部超声筛选出高风险脱机拔管患者,证实了在此类患者中使用经鼻高流量氧疗(HFNC)较常规氧疗可以降低重新插管率,减少ICU住院时间,明显改善患者的呼吸、循环及氧合情况。该临床研究为单中心前瞻性对照研究,但样本量较少,统计存在一定的偏倚,还需要大样本的临床多中心对照研究进一步验证。另外,肺部超声由主治医师床边操作完成,虽然所有操作医师都经过相关肺部超声技能培训,但仍存在超声评分因不同操作人员评估而存在诊断偏差可能。
| [1] | Roca O, Riera J, Torres F, et al. High-flow oxygen therapy in acute respiratory failure[J]. Respir Care, 2010, 55(4): 408-413. DOI:10.1097/cpm.0b013e3182514f29 |
| [2] | Sztrymf B, Messika J, Bertrand F, et al. Beneficial effects of humidified high flow nasal oxygen in critical care patients: a prospective pilot study[J]. Intensive Care Med, 2011, 37(11): 1780-1786. DOI:10.1007/s00134-011-2354-6 |
| [3] | Maggiore SM, Idone FA, Vaschetto R, et al. Nasal high-flow versus Venturi mask oxygen therapy after extubation. Effects on oxygenation, comfort, and clinical outcome[J]. Am J Respir Crit Care Med,, 2014, 190(3): 282-288. DOI:10.1164/rccm.201402-0364OC |
| [4] | Parke R, McGuinness S, Dixon R, et al. Open-label, phase Ⅱ study of routine high-flow nasal oxygen therapy in cardiac surgical patients[J]. Br J Anaesth, 2013, 111(6): 925-931. DOI:10.1093/bja/aet262 |
| [5] | Arbelot C, Ferrari F, Bouhemad B, et al. Lung ultrasound in acute respiratory distress syndrome and acute lung injury[J]. Curr Opin Crit Care, 2008, 14(1): 70-74. DOI:10.1097/MCC.0b013e3282f43d05 |
| [6] | Bouhemad B, Brisson H, Le-Guen M, et al. Bedside ultrasound assessment of positive end-expiratory pressure-induced lung recruitment[J]. Am J Respir Crit Care Med, 2011, 183(3): 341-347. DOI:10.1164/rccm.201003-0369OC |
| [7] | Soummer A, Perbet S, Brisson H, et al. Ultrasound assessment of lung aeration loss during a successful weaning trial predicts postextubation distress*[J]. Crit Care Med, 2012, 40(7): 2064-2072. DOI:10.1097/CCM.0b013e31824e68ae |
| [8] | Salam A, Tilluckdharry L, Amoateng-Adjepong Y, et al. Neurologic status, cough, secretions and extubation outcomes[J]. Intensive Care Med, 2004, 30(7): 1334-1339. DOI:10.1007/s00134-004-2231-7 |
| [9] | Saugel B, Rakette P, Hapfelmeier A, et al. Prediction of extubation failure in medical intensive care unit patients[J]. J Crit Care, 2012, 27(6): 571-577. DOI:10.1016/j.jcrc.2012.01.010 |
| [10] | Brown CV, Daigle JB, Foulkrod KH, et al. Risk factors associated with early reintubation in trauma patients: a prospective observational study[J]. J Trauma, 2011, 71(1): 37-41. DOI:10.1097/TA.0b013e31821e0c6e |
| [11] | Coplin WM, Pierson DJ, Cooley KD, et al. Implications of extubation delay in brain-injured patients meeting standard weaning criteria[J]. Am J Respir Crit Care Med, 2000, 161(5): 1530-1536. DOI:10.1164/ajrccm.161.5.9905102 |
| [12] | Maggiore SM, Idone FA, Vaschetto R, et al. Nasal high-flow versus Venturi mask oxygen therapy after extubation. Effects on oxygenation, comfort, and clinical outcome[J]. Am J Respir Crit Care Med, 2014, 190(3): 282-288. DOI:10.1164/rccm.201402-0364OC |
| [13] | Parke R, McGuinness S, Dixon R, et al. Open-label, phase Ⅱ study of routine high-flow nasal oxygen therapy in cardiac surgical patients[J]. Br J Anaesth, 2013, 111(6): 925-931. DOI:10.1093/bja/aet262 |
| [14] | Corley A, Bull T, Spooner AJ, et al. Direct extubation onto high-flow nasal cannulae post-cardiac surgery versus standard treatment in patients with a BMI ≥30: a randomised controlled trial[J]. Intensive Care Med, 2015, 41(5): 887-894. DOI:10.1007/s00134-015-3765-6 |
| [15] | Gardelli G, Feletti F, Gamberini E, et al. Using sonography to assess lung recruitment in patients with acute respiratory distress syndrome[J]. Emerg Radiol, 2009, 16(3): 219-221. DOI:10.1007/s10140-008-0734-1 |
| [16] | Tsubo T, Yatsu Y, Tanabe T, et al. Evaluation of density area in dorsal lung region during prone position using transesophageal echocardiography[J]. Crit Care Med, 2004, 32(1): 83-87. DOI:10.1097/01.CCM.0000104944.18636.B2 |
| [17] | Agricola E, Picano E, Oppizzi M, et al. Assessment of stress-induced pulmonary interstitial edema by chest ultrasound during exercise echocardiography and its correlation with left ventricular function[J]. J Am Soc Echocardiogr, 2006, 19(4): 457-463. DOI:10.1016/j.echo.2005.11.013 |
| [18] | Fagenholz PJ, Gutman JA, Murray AF, et al. Chest ultrasonography for the diagnosis and monitoring of high-altitude pulmonary edema[J]. Chest, 2007, 131(4): 1013-1018. DOI:10.1378/chest.06-1864 |
| [19] | Noble VE, Murray AF, Capp R, et al. Ultrasound assessment for extravascular lung water in patients undergoing hemodialysis. Time course for resolution[J]. Chest, 2009, 135(6): 1433-1439. DOI:10.1378/chest.08-1811 |
| [20] | Volpicelli G, Caramello V, Cardinale L, et al. Bedside ultrasound of the lung for the monitoring of acute decompensated heart failure[J]. The American Journal of Emergency Medicine, 2008, 26(5): 585-591. DOI:10.1016/j.ajem.2007.09.014 |
| [21] | Hernández G, Vaquero C, González P, et al. Effect of Postextubation High-Flow Nasal Cannula vs Conventional Oxygen Therapy on Reintubation in Low-Risk Patients: A Randomized Clinical Trial[J]. JAMA, 2016, 315(13): 1354-1361. DOI:10.1001/jama.2016.2711 |
| [22] | Hernández G, Vaquero C, Colinas L, et al. Effect of Postextubation High-Flow Nasal Cannula vs Noninvasive Ventilation on Reintubation and Postextubation Respiratory Failure in High-Risk Patients: A Randomized Clinical Trial[J]. JAMA, 2016, 316(15): 1565-1574. DOI:10.1001/jama.2016.14194 |
 2018, Vol. 27
2018, Vol. 27




