念珠菌血症(candidemia)是由念珠菌引起的侵袭性血流感染,随着大剂量广谱抗生素和抗肿瘤药物的长期应用、有创诊疗技术的广泛开展以及感染艾滋病等免疫低下患者的不断增多,其发病率和致死率明显升高。血培养是诊断侵袭性血流感染的金标准,但其灵敏度低,周期长,有研究表明其对念珠菌血症的漏检率高达50%[1]。降钙素原(PCT)是降钙素的前体,正常情况下其在外周血中含量很低,在细菌脂多糖和细胞因子的诱导下释放增加,其作为血流感染诊断治疗和预后的血清学标志物得到越来越广泛的关注[2]。目前PCT对侵袭性血流感染的研究较少,关于其在念珠菌血症的诊断价值尚存争议[2-3]。本研究旨在探讨PCT水平在念珠菌血流感染患者中的临床应用价值。
1 资料与方法 1.1 一般资料本研究选取2013年6月至2017年6月天津医科大学总医院同时送检血液培养和血清PCT检测住院患者783例,其中血培养阴性患者510例。念珠菌组纳入标准符合《侵袭性真菌感染的诊断标准与治疗原则》规定的确诊标准。共收集有效血培养念珠菌阳性121例(念珠菌组),男性75例,女性46例,年龄(70.3±18.7)岁;选择同期细菌血流感染阳性患者152例(细菌组),男性86例,女性66例,年龄(63.4±21.9)岁。排除标准:急性外伤、大面积烧伤、急性心肌梗死、有甲状腺癌及肺小细胞癌病史及病例资料严重缺失的患者[4]。对两组患者的基础疾病,住院时间及病死率等临床资料进行比较。
1.2 检测方法 1.2.1 血培养使用抗菌药物前无菌采集血液标本送检,将血培养瓶置于美国BD BactecTMFX血培养仪中, 血培养瓶报阳者进行革兰染色镜检,根据其形态学特点将一级血培养结果报告临床,再转种到血琼脂平皿或沙氏平皿上,取单个纯培养菌落于法国梅里埃VITEK-2 COMPACT全自动微生物鉴定分析仪上进行菌种鉴定。
1.2.2 PCT所有患者PCT与血培养送检时间间隔在24 h内,结合一步免疫测定夹心法和最终酶联免疫荧光法(ELFA)原理,应用法国梅里埃全自动VIDAS荧光免疫分析仪及专用配套试剂盒对PCT进行检测,检出限为0.05 ng/mL,推荐阳性临界值为0.5 ng/mL。
1.3 统计学方法应用SPSS 20.0软件进行统计分析,绘图采用软件GraphPad prism 5.0。正态分布计量资料用均数±标准差(x±s)表示,组间比较采用独立样本t检验,偏态分布计量资料用M(P25,P75)表示,两组间比较采用Mann-Whitney U检验,多组间比较采用Kruskal-wallis检验,并通过Whisker箱图显示各组PCT检测结果。PCT的截断值及诊断性能采用ROC曲线进行分析。通过单因素和多因素logistic回归分析计算念珠菌血流感染相关因素的OR值和95%CI。以P < 0.05为差异有统计学意义。
2 结果 2.1 患者一般临床资料结果比较念珠菌与细菌血流感染组患者在性别组成上相似,两组患者的血液病、2型糖尿病、急性胰腺炎及脓毒症等基础疾病患病率的差异无统计学意义(P > 0.05)。和细菌血流感染患者相比,念珠菌血症患者平均年龄较大,且入住重症监护病房(ICU)的危重症患者居多(均P < 0.01)。念珠菌感染组罹患肺部感染、呼吸衰竭、慢性肾功能不全等基础疾病,接受有创诊疗包括机械通气、尿管、中心静脉插管以及近3个月内实施手术的患者较细菌血流感染组多,其他相关因素如全胃肠外营养,血液标本采集前使用免疫抑制剂及广谱抗生素,住院时间超过4周和感染病死率的差异均有统计学意义(均P < 0.05)。见表 1。
| 指标 | 念珠菌组 | 细菌组 | t/χ2值 | P值 |
| 年龄(岁,x±s) | 70.3±18.7 | 63.4±21.9 | -2.755 | 0.006 |
| 男性 | 75(62.0) | 86(56.6) | 0.813 | 0.367 |
| 是否入住ICU | 97(80.2) | 65(42.8) | 39.061 | 0.000 |
| 基础疾病 | ||||
| 血液病 | 21(17.4) | 18(11.8) | 1.672 | 0.196 |
| 2型糖尿病 | 39(32.2) | 41(27.0) | 0.899 | 0.343 |
| 急性胰腺炎 | 4(3.3) | 4(2.6) | 0.001 | 0.974 |
| 肺部感染 | 87(71.9) | 84(55.3) | 7.969 | 0.005 |
| 呼吸衰竭 | 67(55.4) | 47(30.9) | 16.561 | 0.000 |
| 慢性肾功能不全 | 57(47.1) | 51(33.6) | 5.177 | 0.023 |
| 脓毒症 | 53(43.8) | 55(36.2) | 1.635 | 0.201 |
| 中心静脉插管 | 47(38.8) | 28(18.4) | 14.101 | 0.000 |
| 尿管 | 109(90.1) | 96(63.2) | 26.112 | 0.000 |
| 机械通气 | 93(76.9) | 38(25.0) | 72.592 | 0.000 |
| 手术(3个月内) | 87(71.9) | 63(41.4) | 25.239 | 0.000 |
| 胃肠外营养 | 105(86.8) | 61(40.1) | 61.506 | 0.000 |
| 免疫抑制剂 | 82(67.8) | 53(34.9) | 29.173 | 0.000 |
| 广谱抗生素 | 119(98.3) | 115(75.7) | 28.324 | 0.000 |
| 住院超过4周 | 71(58.7) | 62(40.8) | 8.629 | 0.003 |
| 病死率 | 35(28.9) | 28(18.4) | 4.188 | 0.041 |
多因素logistic回归分析显示,入住ICU(OR=6.904, 95%CI:3.298~14.452)、机械通气(OR=9.253, 95%CI:3.406~25.138)、全胃肠外营养(OR=4.706, 95%CI:1.948~11.367)、应用免疫抑制剂(OR=2.420, 95%CI:1.205~4.863)及广谱抗生素(OR=6.475, 95%CI:1.182~35.470)是患者罹患念珠菌血症的独立影响因素(均P < 0.05)。
2.2 患者血培养及PCT检测结果783例患者中血培养阴性510例,PCT为0.21(0.06,1.02)ng/mL。念珠菌血流感染121例,PCT为1.15(0.38,6.85)ng/mL。细菌血流感染152例,PCT为2.34(0.77,15.12)ng/mL。所有入选患者血培养阳性273例,其中PCT > 0.5 ng/mL共209例,所占比例为76.6%(209/273),见表 2。
| 组别 | 例数 | PCTa(ng/mL) | PCT阳性(例,%) |
| 细菌组 | 152 | 2.34(0.77, 15.12) | 124(81.58) |
| 念珠菌组 | 121 | 1.15(0.38, 6.85) | 85(70.25) |
| 阴性组 | 510 | 0.21(0.06, 1.02) | 175(34.31) |
| 注:aPCT值为中位数水平,括号内为四分位间距 | |||
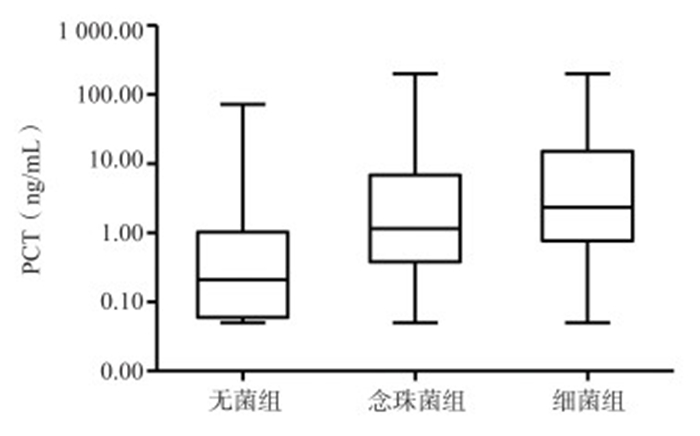
采用Kruskal-wallis检验方法,对表 2中的三组PCT定量检测结果进行分析,得出χ2=156.583,P < 0.01,三组间PCT水平差异有统计学意义。平均秩次为细菌感染组为555.11,念珠菌感染组为493.18,无菌组为319.38;对念珠菌感染组和细菌感染组进行Mann-Whitney U检验,得U=7 491.0,P=0.009,差异有统计学意义,即细菌感染组PCT水平明显高于念珠菌感染组;对念珠菌感染组和无菌组进行Mann-Whitney U检验,得U=16 907.5,P < 0.01,差异有统计学意义(表 2,图 1)。
|
| 图中上下两条线段表示最大值和最小值,箱图的上方和下方表示P75和P25四分位,中间的线段为中位数 图 1 783例患者血培养及PCT检测结果的箱图 Figure 1 Whisker box-plot distribution of procalcitonin values according to the results of blood cultures of 783 patients |
|
|
121例患者念珠菌血流感染阳性且为单一菌株,其中近平滑念珠菌(C.parapsilosis)70例,占念珠菌感染的57.9%,其次为白色念珠菌(C.albicans)21例,热带念珠菌(C.tropicalis)和光滑念珠菌(C.glabrata)均为7例,其他非白念珠菌(non-albicans, NAC)共16例。念珠菌血症患者中PCT阳性85例,阳性比例为70.25%,见表 3。
| 菌种 | 例数 | PCTa[M(P25, P75)ng/mL] | PCT阳性(例, %) |
| 近平滑念珠菌 | 70 | 1.04(0.37, 6.03) | 46(65.71) |
| 白色念珠菌 | 21 | 1.60(0.33, 5.71) | 16(76.19) |
| 无名念珠菌 | 8 | 1.68(0.39, 5.26) | 6(75.00) |
| 热带念珠菌 | 7 | 3.01(1.09, 41.64) | 6(85.71) |
| 光滑念珠菌 | 7 | 1.02(0.58, 17.86) | 6(85.71) |
| 光滑球拟念珠菌 | 6 | 1.16(0.16, 65.55) | 4(66.67) |
| 溶脂念珠菌 | 1 | 13.56b | 1(100.0) |
| 角膜念珠菌 | 1 | 0.09b | 0(0.00) |
| 合计 | 121 | 1.15(0.38, 6.85) | 85(70.25) |
| 注:aPCT值为中位数水平,括号内为四分位间距;b表示只有一株菌,未注明范围 | |||
曲线下面积(AUC)为0.726(95%CI:0.677~0.775)。根据ROC曲线得到的最佳临界值为0.355 ng/mL,此时PCT诊断念珠菌血症的灵敏度为76.86%,特异度为60.78%,约登指数为0.376。见图 2。

|
| 图 2 PCT检测念珠菌血症的ROC曲线 Figure 2 Receiver-operating-characteristic(ROC)curve of procalcitonin for the identification of candidemia |
|
|
念珠菌是引起侵袭性血流感染和深部组织感染的最常见致病菌,是导致危重症患者死亡的重要原因之一。血培养作为血流感染诊断的金标准,由于其自身的局限性不能及时向临床提供诊疗信息。近年来,一些新的血清学诊断方法,包括血浆1, 3-β-D-葡聚糖检测(G试验)、曲霉半乳甘露聚糖抗原测定(GM试验)以及念珠菌芽管(CAGT)抗体试验等应用于临床感染的早期诊断,但具有较高的假阳性率[5]。PCT是由116个氨基酸组成的多肽,在脂多糖和细胞因子的作用下释放增加,而在病毒感染时浓度降低[6-7]。目前PCT已广泛应用于细菌感染的早期诊断及预后评估中,但其在鉴别念珠菌与细菌血流感染应用中的相关报道较少,本研究旨在探讨降钙素原在念珠菌血流感染中的辅助诊断价值。
纳入的273例血流感染阳性患者中,念珠菌感染者121例,细菌感染者152例。念珠菌中白色念珠菌21例,非白念珠菌包括近平滑念珠菌、光滑念珠菌及热带念珠菌的比例较高。在欧洲等国家,近平滑念珠菌是非白念珠菌中最常见的致病菌(约占真菌感染的27.7%)[8],与本研究结果相符。致病菌种由白念到非白念的转变可能与抗真菌药物的普及与侵袭性操作的增加有关[9]。分析结果显示,念珠菌血症患者的血清PCT水平明显低于细菌血流感染患者,念珠菌血流感染患者PCT的ROC曲线结果表明,当界值设定为0.355 ng/mL时血清PCT诊断血流感染念珠菌的灵敏度为76.9%,特异度为60.8%,意大利Pieralli等[2]对非ICU脓毒症患者PCT鉴别诊断念珠菌血症与细菌血流感染的界值报道为2.5 ng/mL,诊断的阴性预测值达到98.3%,相应灵敏度、特异度分别为78.3%、72%,且PCT小于2.5 ng/mL是念珠菌血症的独立相关因素,OR=8.57(95%CI:3.09~23.70,P < 0.01),本研究中80.2%念珠菌血症患者来自ICU,与细菌感染组相比,PCT水平差异也有统计学意义(P < 0.01)。提示对于不同人群以及致病菌引起的血流感染应制定相应的参考值范围。
本研究中念珠菌血症的患者PCT水平低于细菌血流感染者,可能是由于真菌感染释放类型和强度有别于革兰阴性杆菌或革兰阳性菌所诱发的细胞因子以及其他促炎性细胞因子[10-11],且念珠菌感染患者对感染因子免疫应答功能受损,即临床特征为“虚弱表型”[12]。与细菌血流感染的患者相比,念珠菌血症患者平均年龄较大,且入住ICU的危重症患者及罹患肺部感染、呼吸衰竭、慢性肾功能不全等基础疾病居多,全胃肠外营养,使用免疫抑制剂及广谱抗生素,接受有创诊疗及住院时间长等因素差异有统计学意义,念珠菌血症也是在疾病病程后期较为常见。
综上所述,念珠菌是引起真菌血流感染最主要的致病菌,其中又以近平滑念珠菌居多。念珠菌血症患者PCT水平以轻度升高为主,较细菌血流感染患者峰值低,可用于区分真菌及细菌感染[13],Martini等[14]对比念珠菌血症、脓毒血症及混合感染三组患者发现,PCT持续低水平重症患者易发生念珠菌血症, 即血清PCT水平对念珠菌血流感染有一定的辅助诊断价值。对于存在发生念珠菌血症相关因素的患者,若其PCT水平在灰色浓度间起伏且不小于0.355 ng/mL,结合其临床症状及血培养、G试验等实验室检测指标,鉴别诊断是否有念珠菌血流感染,并及时给予有效地经验性抗真菌治疗。
然而,本研究是回顾性病例对照研究,无法对感染患者的PCT水平进行动态监测,以致无法控制其检测时间和疾病病程等混杂因素的影响;PCT可以鉴别念珠菌和细菌血流感染,但不能用于区别真菌感染和定植菌[15];由于侵袭性血流感染的患者较少,需较长时间进行大样本前瞻性队列研究来进一步分析PCT在念珠菌血症早期诊断及预后评估中的应用价值。
| [1] | Clancy CJ, Nguyen MH. Finding the " missing 50%" of invasive candidiasis: how nonculture diagnostics will improve understanding of disease spectrum and transform patient care[J]. Clin Infect Dis, 2013, 56(9): 1284-1292. DOI:10.1093/cid/cit006 |
| [2] | Pieralli F, Corbo L, Torrigiani A, et al. Usefulness of procalcitonin in differentiating Candida, and bacterial blood stream infections in critically ill septic patients outside the intensive care unit[J]. Intern Emerg Med, 2017, 12(5): 629-635. DOI:10.1007/s11739-017-1627-7 |
| [3] | Brodská H, Malíčková K, Adámková V, et al. Significantly higher procalcitonin levels could differentiate; Gram-negative sepsis from Gram-positive and fungal sepsis[J]. Clin Exp Med, 2013, 13(3): 165-170. DOI:10.1007/s10238-012-0191-8 |
| [4] | 赵倩, 谢月群, 张涛, 等. 降钙素原对脓毒症患者病情及预后的临床价值[J]. 中华急诊医学杂志, 2016, 25(7): 937-943. DOI:10.3760/cma.j.issn.1671-0282.2016.07.019 |
| [5] | Cornely OA, Bassetti M, Calandra T, et al. ESCMID* guideline for the diagnosis and management of Candida diseases 2012: non-neutropenic adult patients[J]. Clin Microbiol Infect, 2012, 18(s7): 19-37. DOI:10.1111/1469-0691.12039 |
| [6] | Gilbert DN. Use of plasma procalcitonin levels as an adjunct to clinical microbiology[J]. J Clin Microbiol, 2010, 48(7): 2325-2329. DOI:10.1128/JCM.00655-10 |
| [7] | Assicot M, Gendrel D, Carsin H, et al. High serum procalcitonin concentrations in patients with sepsis and infection[J]. Lancet, 1993, 341(8844): 515-518. DOI:10.1016/0140-6736(93)90277-N |
| [8] | Pfaller MA, Moet GJ, Messer SA, et al. Candida bloodstream infections: comparison of species distributions and antifungal resistance patterns in community-onset and nosocomial isolates in the SENTRY antimicrobial surveillance program, 2008-2009[J]. Antimicrob Agents Chemother, 2011, 55(2): 561-566. DOI:10.1128/AAC.01079-10 |
| [9] | 王昊, 吴大玮, 韩辉, 等. 白念珠菌与非白念珠菌血流感染危险因素、抗菌药物应用及预后比较[J]. 中华传染病杂志, 2014, 32(8): 474-478. DOI:10.3760/cma.j.issn.1000-6680.2014.08.006 |
| [10] | Tavares E, Maldonado R, Ojeda ML, et al. Circulating inflammatory mediators during start of fever in differential diagnosis of gram-negative and gram-positive infections in leukopenic rats[J]. Clin Diag Lab Immunol, 2005, 12(9): 1085-1093. DOI:10.1128/CDLI.12.9.1085–1093.2005 |
| [11] | Linscheid P, Seboek D, Schaer DJ, et al. Expression and secretion of procalcitonin and calcitonin gene-related peptide by adherent monocytes and by macrophage-activated adipocytes[J]. Crit Care Med, 2004, 32(8): 1715-1721. DOI:10.1097/01.CCM.0000134404.63292.71 |
| [12] | Boomer JS, To K, Chang KC, et al. Immunosuppression in patients who die of sepsis and multiple organ failure[J]. JAMA, 2011, 306(23): 2594-605. DOI:10.1001/jama.2011.1829 |
| [13] | 金卫, 张晓燕, 杜江, 等. 危重病科念珠菌血症23例临床分析[J]. 临床荟萃, 2016, 31(11): 1218-1221. DOI:10.3969/J.ISSN.1004-583x.2016.11.014 |
| [14] | Martini A, Gottin L, Menestrina N, et al. Procalcitonin levels in surgical patients at risk of candidemia[J]. J Infect, 2010, 60(6): 425-430. DOI:10.1016/j.jinf.2010.03.003 |
| [15] | Dou YH, Du JK, Liu HL, et al. The role of procalcitonin in the identification of invasive fungal infection-a systemic review and meta-analysis[J]. Diagn Microbiol Infect Dis, 2013, 76(4): 464-469. DOI:10.1016/j.diagmicrobio.2013.04.023 |
 2018, Vol. 27
2018, Vol. 27




