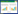自发性脑出血(spontaneous intracerebral hemorrhage, SICH)是脑出血中最具破坏性的亚型,约占所有脑出血病例的80%~85%[1]。其病理生理机制复杂,早期血肿占位效应可直接破坏脑实质结构,而继发性颅内压(intracranial pressure, ICP)升高、炎症级联反应及氧化应激等过程进一步加剧神经功能损伤,显著增加致残率和病死率[2]。研究表明,SICH患者发病后30 d病死率高达40%,幸存者中约75%遗留严重神经功能障碍[3]。因此,早期精准评估神经功能预后,对个体化治疗决策、资源优化分配及改善长期生活质量具有重要意义。
有创颅内压监测(invasive ICP monitoring)被视为评估ICP的金标准,但其临床应用受限于侵入性操作风险(如感染、出血)及高成本,尤其在急诊环境中难以普及[4]。近年来,无创监测技术快速发展,其中超声测量视神经鞘直径(optic nerve sheath diameter, ONSD)因操作简便、可重复性强,成为动态评估ICP的重要工具,近年来受到广泛关注[5]。视神经鞘作为硬脑膜的延伸结构,其直径随ICP升高而扩张,这一现象与蛛网膜下腔脑脊液压力传导密切相关[6]。多项研究证实,ONSD与有创ICP监测结果呈显著正相关(r=0.78~0.92),且ONSD > 5.8 mm可敏感提示颅内高压[7]。然而,单纯依赖ONSD预测神经功能预后的效能仍有争议,可能与个体解剖差异及操作标准化不足有关[8]。另一方面,SICH后的全身炎症反应在继发性脑损伤中扮演关键角色[9]。血肿分解产物激活小胶质细胞,释放白细胞介素-6(interleukin-6, IL-6)、C反应蛋白(C-reactive protein, CRP)等促炎因子,通过破坏血脑屏障、诱导神经元凋亡等机制加重神经损伤[10]。临床观察显示,炎症标志物如中性粒细胞计数(absolute neutrophil count, ANC)、IL-6水平与SICH患者功能预后呈负相关[11]。然而,炎症指标易受感染、应激等复杂因素影响,单独预测预后的特异性不足。
颅内压升高与炎症反应是ICH后脑损伤的两种关键病理机制,二者可能通过协同作用(如炎症介导的血管通透性增加加重脑水肿)影响预后。然而,现有研究多孤立分析单一指标,或未能充分控制血肿体积、位置等传统预后因素的干扰,缺乏对多模态生物标志物(如ONSD联合炎症指标)独立增量预测价值(incremental predictive value)的验证。基于上述背景,本研究拟在控制血肿特征及入院时间等临床变量的基础上,探讨ONSD联合炎症指标(WBC、IL-6等)对SICH患者神经功能预后的预测价值,旨在构建一种无创、动态、多维度的预后评估模型,为早期干预提供理论依据。
1 资料与方法 1.1 研究对象回顾性收集2024年4月至2024年12月在浙江省某三级甲等综合医院急诊抢救室收治的SICH患者。纳入标准:①年龄大于18岁;②确诊为SICH;③入院24 h内完成头颅CT及实验室检查;④具有完整的临床及影像学资料。排除标准:①眼部疾病者(如眼外伤、视神经肿瘤、青光眼等);②颈椎损伤或无法耐受床头抬高30°者;③患者基本信息、临床、影像学及超声资料不全者;④超声图像质量不佳;⑤继发于动脉瘤、血管畸形、肿瘤或抗凝治疗的脑出血。所有患者或家属均签署知情同意书,且有权利在任何阶段退出本研究。本研究通过医院伦理审查。伦理批件号:(2024)伦审研第(1434)号。
本研究使用G*Power 3.1.9.7进行样本量估算,统计分析选择F检验中的多元线性回归,以效应量、α值及统计效能计算样本量。由于本研究为试点研究,故假定效应量I2为0.2,设置α=0.05,统计效能1-β=0.8,计算样本量共需70例。
收集患者的一般资料(年龄、性别、BMI等)、临床资料(格拉斯哥评分、RASS评分等)及入院后第一次检验的外周血炎症指标(WBC、CRP、IL-6等)。其他临床资料包括既往史、是否镇静、是否使用血管活性药物、住院天数、出院CPC评分及外周血全身炎症反应相关指标则由研究者通过电子病历系统进行收集。收集的所有入院头颅CT影像均由两名不知晓患者预后的神经内科医师独立评估,测量血肿体积(使用ABC/2公式)并记录出血位置(深部/脑叶)。同时记录从发病到入院的时间(出血天数)。最终共纳入75例符合标准的患者。根据出院CPC得分将患者分为神经功能预后良好组(CPC≤2,n=26)和神经功能预后不良组(CPC>2,n=49)。
1.2 影像学资料采集CT影像分析与临床变量获取:调取患者入院时首次头颅CT平扫影像。血肿体积采用ABC/2公式计算。出血位置由两名高年资神经科医师盲法判定,分为深部(基底节、丘脑)及脑叶。发病至入院的时间(出血天数)通过病历系统记录。
ONSD测量:患者取仰卧位,头保持正中位,床头抬高30°,双眼睑闭合,眼球尽量保持固定。使用一次性透明敷贴对双眼进行保护,将7.5 MHz超声探头(AIX8)轻放于闭合的上眼睑,不对眼球施加压力。扫描方向分为横断面和矢状面。横断面扫查时,将探头水平方向置于患者闭合的上眼睑;矢状面扫查时,将探头垂直方向置于患者闭合的上眼睑。调整合适的角度,保存双侧视神经鞘最佳成像,对双侧眼球后侧3 mm处视神经鞘进行检查测量。每只眼睛记录两次ONSD值后取所有4次成像的平均值,精确至0.01 mm。ONSD的测量均在患者入院后0.5 h内完成。
1.3 统计学方法采用SPSS25.0统计学软件对数据进行综合分析。所有计量资料均以中位数及四分位间距[M(P25,P75)]表示,符合正态分布采用独立样本t检验、单因素方差分析,不符合正态分布采用Mann-Whitney U检验。计数资料采用频数和百分数[n(%)]表示,使用χ2检验与Fishers精确检验比较组间率差异。将单因素分析中差异有统计学意义的指标纳入二分类多因素Logistic回归,探究各变量对结局指标的预测价值,并绘制受试者操作特征曲线(receiver operator characteristic curve, ROC曲线),分析各项目对神经功能预后的预测效能,计算曲线下面积(area under the curve, AUC)并得出最佳阈值。以Pearson法(正态分布)或Spearman法(非正态分布)计算ONSD与炎症指标的相关性,随后将出血时间、出血位置及出血量作为核心协变量以Enter法纳入回归模型探究ONSD与炎症指标对结局指标的预测价值,并进行共线性分析探究其预测价值是否相互独立。共线性分析中容忍度>0.2、VIF<5即视为不存在共线性。以P<0.05为差异有统计学意义。
2 结果 2.1 一般资料对比本研究将患者的基本资料包括年龄、性别、身高、体重、高血压、糖尿病及高脂血症住院时长等进行统计分析发现,两组性别及年龄差异无统计学意义(P>0.05),见表 1。
| 项目 | 预后不良组(n=49) | 预后良好组(n=26) | Z/χ2/F值 | P值 |
| 年龄(岁) | 62(50.5,76) | 55.5(47.5,66) | 1.199 | 0.082 |
| BMI | 23.44(21.33,26.19) | 23.61(21.96,26.83) | 1.952 | 0.793 |
| 性别 | 0.421 | 0.516a | ||
| 男 | 32(68.09) | 15(31.91) | ||
| 女 | 17(60.71) | 11(39.29) | ||
| 合并高血压 | 26(56.52) | 20(43.48) | 4.078 | 0.043b |
| 合并糖尿病 | 7(58.33) | 5(41.67) | 0.309 | 0.578b |
| 合并高脂血症 | 0(00.00) | 1(100.00) | 1.910 | 0.167b |
| 住院时长(d) | 12(4,23) | 10(6,15.5) | 1.359 | 0.466 |
| 注:a为χ2检验;b为Fisher's exact test,其他为独立样本T检验 | ||||
选取了SICH患者入院后第一次血液检验指标,单因素回归分析显示,神经功能预后良好组与预后不良组的ONSD平均值、血清WBC及ANC差异有统计学意义(P<0.05),同时,对可能影响预后的传统影像学与临床指标进行了分析,发现预后不良组的血肿体积显著大于预后良好组(P=0.001),而两组在出血位置(深部/脑叶)以及出血时间(急性期/亚急性期)上均差异无统计学意义(P>0.05)见表 2。
| 项目 | 预后不良组(n=49) | 预后良好组(n=26) | Z/χ2/F值 | P值 |
| 连续变量 | ||||
| ONSD平均值/mm | 5.95±0.06 | 5.54±0.32 | 9.310 | 0.002 |
| WBC/109/L | 13.67±4.76 | 8.76±2.41 | 5.554 | 0.000 |
| MONO/109/L | 0.59±0.28 | 0.49±0.16 | 7.367 | 0.114 |
| ANC/109/L | 13.93±12.18 | 6.91±2.36 | 3.592 | 0.005 |
| ALC/109/L | 1.27±0.79 | 1.27±0.62 | 1.050 | 0.965 |
| CRP /mg/L | 45.56±65.52 | 21.21±36.98 | 4.781 | 0.084 |
| PCT/ng/mL | 1.98±0.60 | 0.22±0.40 | 2.295 | 0.386 |
| IL-6/pg/mL | 273.54±992.40 | 9.26±20.58 | 5.137 | 0.180 |
| 分类变量 | ||||
| 出血量(n, %) | -3.366 | 0.001b | ||
| <30 mL | 14(24.00) | 18(10.70) | ||
| ≥30 mL | 35(46.70) | 8(18.60) | ||
| 出血天数(n, %) | -0.321 | 0.748b | ||
| 急性期 | 32(42.70) | 16(21.30) | ||
| 亚急性期 | 17(22.70) | 10(13.30) | ||
| 出血位置(n, %) | 0.751 | 0.386a | ||
| 深部组 | 33(44.00) | 20(26.70) | ||
| 脑叶组 | 16(21.30) | 6(8.00) | ||
| 注:a为χ2检验;b为Mann-Whitney U test,其他为独立样本T检验 | ||||
多因素logistic回归分析结果(表 3)显示,在调整了相关混杂因素后,ONSD平均值、血清WBC、ANC及IL-6仍是SICH患者神经功能预后不良的独立危险因素。为进一步验证ONSD与炎症指标的独立预测价值,构建了包含传统预后因素(出血时间、出血位置、血肿体积)的多元logistic回归模型(表 5)。Model 1(调整出血时间、位置、血肿体积+ONSD+ANC)和Model 2(调整出血时间、位置、血肿体积+ONSD+WBC)分析表明,在纳入传统因素后,ONSD(OR=9.237, P=0.009; OR=6.437, P=0.017)与炎症指标(ANC, P<0.001; WBC, P<0.001)仍是预后的强预测因子。Model 3(调整出血时间、位置、血肿体积+ONSD+IL-6)同样显示ONSD(OR=6.176, P=0.019)与IL-6(OR=1.078, P=0.002)的预测价值保持独立。同时分析ONSD平均值+WBC+IL-6+ANC的预测效能后,结果显示:ONSD平均值、外周血血清中WBC、IL-6、ANC单独预测SICH患者预后的曲线下面积(AUC)分别为0.717、0.835、0.932、0.860。联合三项指标后预测患者预后的ROC曲线下的面积为0.939(95%CI: 0.882~0.996),联合预测效能更高。见表 4,图 1。
| 项目 | B | SE | Wald | P值 | OR值 | 95%CI | |
| 下限 | 上限 | ||||||
| WBC | 0.459 | 0.117 | 15.282 | 0.000 | 1.583 | 1.257 | 1.993 |
| ANC | 0.503 | 0.128 | 15.345 | 0.000 | 1.653 | 1.286 | 2.126 |
| IL-6 | 0.073 | 0.024 | 9.663 | 0.002 | 1.076 | 1.028 | 1.127 |
| ONSD平均值 | 1.657 | 0.573 | 8.349 | 0.004 | 5.244 | 1.704 | 16.135 |
| 常量 | -16.055 | 5.545 | 8.382 | 0.004 | 0.000 | ||
| 指标 | 临界值 | AUC | 约登指数 | 敏感度(%) | 特异度(%) | 95%CI | |
| 下限 | 上限 | ||||||
| WBC | 12.400 | 0.835 | 0.513 | 55.10 | 96.20 | 0.746 | 0.924 |
| ANC | 9.130 | 0.860 | 0.584 | 77.60 | 80.80 | 0.778 | 0.942 |
| IL-6 | 10.25 | 0.932 | 0.844 | 95.90 | 88.50 | 0.856 | 1.000 |
| ONSD平均值 | 5.972 | 0.717 | 0.493 | 53.10 | 96.20 | 0.604 | 0.830 |
| 联合检测 | 0.384 | 0.939 | 0.788 | 98.00 | 80.80 | 0.882 | 0.996 |
| 项目 | B | SE | Wald | P值 | OR值 | 95%CI | 共线性统计 | ||
| 下限 | 上限 | 容差 | VIF | ||||||
| Model 1 | |||||||||
| 常量 | -19.713 | 6.089 | 10.481 | 0.001 | 0.000 | ||||
| 出血天数 | -0.179 | 0.784 | 0.052 | 0.820 | 0.836 | 0.180 | 3.892 | 0.937 | 1.068 |
| 出血位置 | 0.975 | 0.774 | 1.588 | 0.208 | 2.652 | 0.582 | 12.093 | 0.908 | 1.101 |
| 出血量 | 1.392 | 0.736 | 3.574 | 0.059 | 4.022 | 0.950 | 17.022 | 0.892 | 1.121 |
| ONSD平均值 | 2.512 | 0.930 | 7.305 | 0.007 | 12.336 | 1.995 | 76.287 | 0.905 | 1.105 |
| ANC | 0.564 | 0.163 | 11.949 | 0.001 | 1.758 | 1.277 | 2.421 | 0.861 | 1.162 |
| Model 2 | |||||||||
| 常量 | -16.531 | 5.338 | 9.590 | 0.001 | 0.000 | ||||
| 出血天数 | 0.415 | 0.787 | 0.278 | 0.598 | 1.514 | 0.324 | 7.078 | 0.955 | 1.047 |
| 出血位置 | 0.572 | 0.740 | 0.597 | 0.440 | 1.771 | 0.415 | 7.555 | 0.904 | 1.106 |
| 出血量 | 2.132 | 0.749 | 8.105 | 0.004 | 8.429 | 1.943 | 36.571 | 0.897 | 1.114 |
| ONSD平均值 | 1.855 | 0.833 | 4.960 | 0.026 | 6.391 | 1.249 | 32.694 | 0.876 | 1.142 |
| WBC | 0.485 | 0.141 | 11.795 | 0.001 | 1.623 | 1.231 | 2.14 | 0.882 | 1.134 |
| Model 3 | |||||||||
| 常量 | -12.817 | 4.743 | 7.302 | 0.007 | 0.000 | ||||
| 出血天数 | 0.066 | 0.863 | 0.006 | 0.939 | 1.068 | 0.197 | 5.792 | 0.946 | 1.057 |
| 出血位置 | -0.242 | 0.771 | 0.099 | 0.753 | 0.785 | 0.173 | 3.555 | 0.912 | 1.097 |
| 出血量 | 1.433 | 0.709 | 4.082 | 0.043 | 4.190 | 1.044 | 16.818 | 0.909 | 1.100 |
| ONSD平均值 | 1.981 | 0.807 | 6.031 | 0.014 | 7.252 | 1.492 | 35.252 | 0.888 | 1.127 |
| IL-6 | 0.065 | 0.023 | 8.276 | 0.004 | 1.067 | 1.021 | 1.116 | 0.911 | 1.097 |
|
| 图 1 ONSD、WBC、IL-6、ANC及联合检测在SICH患者预后的ROC曲线 Fig 1 ROC curves of ONSD, WBC, IL-6, ANC and their combination for predicting prognosis in SICH patients |
|
|
本研究中,预后不良组的WBC水平显著升高[(13.67±4.76)×109/L],提示炎症反应的强度与神经功能预后呈负相关。WBC的升高可能通过多种机制加剧脑损伤。白细胞浸润脑组织后,释放大量促炎因子(如IL-6、TNF-α)和活性氧(ROS),导致血脑屏障破坏和神经元凋亡[12],并且中性粒细胞作为WBC的主要成分,其浸润可进一步加重脑水肿和神经功能损害。现有研究表明,中性粒细胞通过释放基质金属蛋白酶(MMPs)和髓过氧化物酶(MPO),破坏血管基底膜,增加血脑屏障通透性,进而加重脑水肿[13]。不仅如此,WBC的升高还可能通过激活小胶质细胞,促进炎症级联反应的持续放大。小胶质细胞是中枢神经系统的主要免疫细胞,其在SICH后被激活,释放大量促炎因子,进一步加剧神经炎症反应[14]。因此,WBC的升高不仅是炎症反应的标志,还可能直接参与脑损伤的病理过程。中性粒细胞的浸润与血肿周围水肿(PHE)的形成密切相关。PHE是SICH后常见的继发性损伤,其严重程度与神经功能预后密切相关[15]。中性粒细胞通过释放ROS和MMPs,破坏血脑屏障,增加血管通透性,进而加重PHE[16]。因此,ANC的升高不仅是炎症反应的标志,还可能直接参与PHE的形成和神经功能损害的加重。
IL-6是炎症反应中的关键介质,在SICH后的脑损伤中发挥了重要作用。本研究中,预后不良组的IL-6水平显著高于预后良好组[(273.54±992.40) pg/mL vs. (9.26±20.58)pg/mL],提示IL-6的升高与神经功能预后密切相关。IL-6通过激活JAK-STAT信号通路,促进血脑屏障破坏和神经元凋亡[17]。此外,IL-6还可通过诱导小胶质细胞活化,进一步加剧神经炎症反应。IL-6的升高还与SICH后的继发性脑损伤密切相关。有实验证明,IL-6水平与血肿周围水肿(PHE)的严重程度呈正相关[18]。IL-6通过增加血管通透性和诱导神经元凋亡,加重PHE和神经功能损害[4]。此外,IL-6还可通过激活NF-κB信号通路,促进炎症因子的持续释放,形成炎症级联反应的恶性循环[18]。
尽管本研究中CRP水平在预后不良组和预后良好组之间差异无统计学意义(P=0.110),但其在炎症反应中的作用仍不可忽视。CRP是急性期反应蛋白,其水平在炎症反应早期升高,但由于其半衰期较长(约19 h),可能在急性期反应中滞后于IL-6等快速反应标志物。研究表明,CRP水平与SICH后的神经功能预后呈负相关,但其预测价值可能受到检测时间点的影响[7]。因此,未来研究需动态监测CRP水平的变化趋势,以更准确地评估其与神经功能预后的关系。
本研究通过多元回归模型控制了血肿体积、出血位置及出血时间等传统预后因素的影响,结果表明ONSD、WBC、ANC与IL-6是独立于这些传统因素的预测指标。这一发现强化了ONSD与全身炎症反应在SICH病理进程中的核心作用,其预测价值并非由血肿的物理特性(如大小、位置)或出血时间所驱动。单因素分析显示较大的血肿体积与不良预后显著相关,这与既往研究[3-4]一致,但出血位置(深部或脑叶)及出血时间(急性期或亚急性期)在本队列中并未显示出显著的预后区分能力。这可能与本研究的样本量相对较小有关,未来需要更大样本的研究进一步验证。然而,即使在调整了这些传统因素后,ONSD与炎症标志物仍保持其强大的独立预测能力,这凸显了将颅内压无创监测与全身炎症状态评估相结合,对于构建多维预后评估模型具有重要的增量价值(incremental value)。
尽管本研究揭示了炎症指标与神经功能预后的相关性,但仍存在一些局限性。首先,未动态监测炎症指标的变化趋势,难以评估时间维度对预后的影响。第二,未收集患者在入院前是否使用脱水药物或降颅压药物等可能引起ONSD改变的资料,难以排除院前药物对ONSD与结局的影响;最后,由于本研究是单中心回顾性试点研究,样本量较小(n=75),可能存在选择偏倚,且内部验证的过拟合风险较高,同时难以开展外部验证,应审慎对待研究结论。未来需开展多中心前瞻性队列研究,结合影像学参数(如血肿体积、中线移位)及分子标志物(如GFAP、S100β),进一步明确OSND与炎症指标在SICH患者中的联合预测价值。
总之,本研究表明,ONSD联合全身炎症反应相关指标(WBC、IL-6等)对SICH患者神经功能预后具有较高的预测价值。联合检测可显著提高预测效能(AUC=0.939),为临床提供一种无创、简便的预后评估方法,有助于早期识别高危患者并采取相应的干预措施。
利益冲突声明 文中测量视神经鞘直径所用的仪器为便携式多普勒超声诊断仪(型号:AIX 8),生产公司为深圳市理邦精密仪器股份有限公司,产地中国,由医院统一采购,本研究未接受任何可能影响结果解释的商业或财务资助。所有作者均无与本研究相关的经济利益或其他潜在利益冲突
作者贡献声明 王冰祥、王钰炜、王飒:酝酿和设计实验、实施研究、分析/解释数据,王冰祥:起草文章、统计学分析,王钰炜、王飒、王美玲、许书荣:对文章的知识性内容作批评性审阅,刘亚洁、周帅帅、吴青峰:数据收集及整理
| [1] | Aguilar M, Freeman WD. Spontaneous intracerebral hemorrhage[J]. Semin Neurol, 2010, 30(5): 555-564. DOI:10.1055/s-0030-1268865 |
| [2] | Keep RF, Hua Y, Xi GH. Intracerebral haemorrhage: mechanisms of injury and therapeutic targets[J]. Lancet Neurol, 2012, 11(8): 720-731. DOI:10.1016/s1474-4422(12)70104-7 |
| [3] | Hemphill JC Ⅲ, Greenberg SM, Anderson CS, et al. Guidelines for the management of spontaneous intracerebral hemorrhage: a guideline for healthcare professionals from the American heart association/American stroke association[J]. Stroke, 2015, 46(7): 2032-2060. DOI:10.1161/str.0000000000000069 |
| [4] | Raboel PH, Bartek J, Andresen M, et al. Intracranial pressure monitoring: invasive versus non-invasive methods: a review[J]. Crit Care Res Pract, 2012, 2012: 950393. DOI:10.1155/2012/950393 |
| [5] | Kim DH, Jun JS, Kim R. Ultrasonographic measurement of the optic nerve sheath diameter and its association with eyeball transverse diameter in 585 healthy volunteers[J]. Sci Rep, 2017, 7: 15906. DOI:10.1038/s41598-017-16173-z |
| [6] | Hansen HC, Helmke K. Validation of the optic nerve sheath response to changing cerebrospinal fluid pressure: ultrasound findings during intrathecal infusion tests[J]. J Neurosurg, 1997, 87(1): 34-40. DOI:10.3171/jns.1997.87.1.0034 |
| [7] | Robba C, Cardim D, Tajsic T, et al. Ultrasound non-invasive measurement of intracranial pressure in neurointensive care: a prospective observational study[J]. PLoS Med, 2017, 14(7): e1002356. DOI:10.1371/journal.pmed.1002356 |
| [8] | Maissan IM, Dirven PJAC, Haitsma IK, et al. Ultrasonographic measured optic nerve sheath diameter as an accurate and quick monitor for changes in intracranial pressure[J]. J Neurosurg, 2015, 123(3): 743-747. DOI:10.3171/2014.10.jns141197 |
| [9] | 任礽, 蔡菁. 重症神经颅腔动力学Monro-Kellie概念的变迁: 颅高压管理从数字到范式的转变[J]. 中华急诊医学杂志, 34(12): 1653-6. DOI:10.3760/cma.j.cn114656-20251113-00776 |
| [10] | 中国医师协会急诊医师分会. 急性脑损伤生物标志物临床应用专家共识[J]. 中华急诊医学杂志, 2025, 34(12): 1662-79. DOI:10.3760/cma.j.cn114656-20251119-00822 |
| [11] | Wang ZG, Gong QY, Guo C, et al. Neutrophil-to-lymphocyte ratio predicts hematoma growth in intracerebral hemorrhage[J]. J Int Med Res, 2019, 47(7): 2970-2975. DOI:10.1177/0300060519847866 |
| [12] | 谷天艳, 潘镜余, 陈玲, 等. 炎性细胞因子TNF-α、IL-6、IL-8预测新发脑出血患者预后的价值[J]. 诊断学理论与实践, 23(4): 405-15. DOI:10.16150/j.1671-2870.2024.04.009 |
| [13] | Wang J, Doré S. Inflammation after intracerebral hemorrhage[J]. J Cereb Blood Flow Metab, 2007, 27(5): 894-908. DOI:10.1038/sj.jcbfm.9600403 |
| [14] | Perera MN, Ma HK, Arakawa S, et al. Inflammation following stroke[J]. J Clin Neurosci, 2006, 13(1): 1-8. DOI:10.1016/j.jocn.2005.07.005 |
| [15] | Shrestha B, Shrestha P, Ghale P, et al. Correlation between invasive intracranial pressure monitoring and optic nerve sheath diameter in patients with traumatic brain injury[J]. Kathmandu Univ Med J, 2022, 19(2): 221-224. DOI:10.3126/kumj.v19i2.49650 |
| [16] | Bäuerle J, Lochner P, Kaps M, et al. Intra- and interobsever reliability of sonographic assessment of the optic nerve sheath diameter in healthy adults[J]. J Neuroimaging, 2012, 22(1): 42-45. DOI:10.1111/j.1552-6569.2010.00546.x |
| [17] | Rhodes A, Wort SJ, Thomas H, et al. Plasma DNA concentration as a predictor of mortality and sepsis in critically ill patients[J]. Crit Care, 2006, 10(2): R60. DOI:10.1186/cc4894 |
| [18] | Dubourg J, Javouhey E, Geeraerts T, Messerer M, Kassai B. Ultrasonography of optic nerve sheath diameter for detection of raised intracranial pressure: a systematic review and meta-analysis[J]. Intensive Care Med, 2011, 37(7): 1059-68. DOI:10.1007/s00134-011-2224-2 |
 2026, Vol. 35
2026, Vol. 35