2. 首都医科大学康复医学院,中国康复研究中心北京博爱医院心血管内科,北京 100068;
3. 保定市康复医院呼吸内科,保定 071051;
4. 首都医科大学附属北京朝阳医院急诊医学中心,心肺脑复苏北京市重点实验室,北京 100020;
5. 首都医科大学石景山教学医院北京市石景山医院急诊科,北京 100043
2. Cardiovascular Department, Beijing Bo'Ai Hospital, China Rehabilitation Research Center, Capital Medical University School of Rehabilitation Medicine, Beijing 100068, China;
3. Respiratory Department, Baoding Rehabilitation Hospital, Baoding 071051, China;
4. Emergency Medicine Clinical Center, Beijing Chao-Yang Hospital, Capital Medical University, Beijing Key Laboratory of Cardiopulmonary Cerebral Resuscitation, Beijing 100020, China;
5. Department of Emergency Medicine, Shijingshan Teaching Hospital of Capital Medical University, Beijing Shijingshan Hospital, Beijing 100043, China
当前世界各地的人口都在加速老龄化,随着该问题的加剧,WHO提出健康老龄化的概念是指发展和维护老年健康生活所需的功能发挥的过程[1]。衰弱是一种与年龄增长相关的老年综合征,其特征是生理储备功能下降,对应激源的易感性增加,导致谵妄、跌倒、失能、住院、死亡等临床负性结局增加[2-5]。据Meta分析报道,全球社区老年人衰弱的患病率18.8%[6],中国社区老年人衰弱患病率10.1%[7],已成为健康老龄化的重要阻碍。老年人衰弱常因急性疾病打破之前的平衡而被发现,这些患者往往因为急性疾病就诊于急诊科[8]。美国国立卫生院老年研究所衰弱工作组2017年召开的“将衰弱整合到临床实践”专题讨论会提出衰弱用于急诊、危重症患者等临床实践中[9]。已有研究证实衰弱的快速评估能预测预后,为个体化医疗照护提供依据[10-11],但关于哪种衰弱筛查工具更适用于急诊,目前尚无定论。我国老龄化进程开始较晚,衰弱的研究主要集中于社区人群和住院患者。急诊医生对衰弱关注较少,衰弱筛查在急诊尚未普及。因此笔者进行了该研究,采用衰弱筛查问卷(frailty screening questionnaire, FSQ)[9]、衰弱(FRAIL)量表[12]、临床衰弱量表(clinical frailty scale, CFS)[13]在急诊科老年患者中进行衰弱筛查,比较其对预后的预测效能,验证适用于急诊科的衰弱筛查工具。
1 资料与方法 1.1 研究对象本研究为前瞻性队列研究,纳入2021年1月至12月于北京博爱医院急诊科治疗的老年患者为研究对象。纳入标准:(1)年龄≥60岁;(2)因急性病发生急诊。排除标准:(1)不能配合完成评估;(2)需行急诊手术;(3)住院时间小于24 h;(4)临床资料不完整。所有患者均按照急诊科诊疗常规路径进行治疗。
本研究获得中国康复研究中心医学伦理委员会批准(2021-093-1);所有入选患者同意参加本研究并签署知情同意书。
1.2 研究方法 1.2.1 一般资料收集收集所有入选患者的人口统计学资料,包括性别、年龄、身体质量指数(body mass index, BMI)、受教育水平等;记录患者急诊就诊的主要疾病及共患病,疾病诊断基于国际疾病分类第十版。
1.2.2 衰弱量表评定入院24 h内对入选患者进行FSQ、FRAIL、CFS评分,依据各评分标准分别将患者分为衰弱组、无衰弱组。
1.2.3 终点事件随访主要终点:患者12个月内全因死亡。次要终点:患者12个月内失能、12个月内再次发生急诊。采用Barthel指数进行日常生活能力评定,以Barthel指数≤60定义失能。
所有量表评估由2名经过培训的急诊科主治医师完成。
1.3 统计学方法采用SPSS 27.0、MedCalc 15.2和GraphPad Prism 9.4统计软件进行数据分析和画图。采用受试者工作特征(receiver operating characteristic, ROC)曲线评价3种衰弱评分对终点事件的预测能力,计算并比较曲线下面积(area under the curve, AUC)和95%置信区间(confidence interval, CI)。分别绘制依据FSQ、FRAIL、CFS 3种标准衰弱组与无衰弱组的Kaplan-Meier生存曲线,应用Log-rank法进行生存比较;采用Cox风险比例回归模型分析衰弱对患者12个月病死率的影响,相对危险度用风险比(hazard ratio, HR)和95%CI表示。以P < 0.05为差异有统计学意义。
2 结果 2.1 研究人群基本资料共纳入406例急诊老年患者,年龄60~97岁,中位年龄80岁;其中男性212例、女性194例,男女比例为1.1∶1.0;中位受教育水平为小学;患者急诊就诊的主要急性病构成为:肺炎154例(37.9%)、急性脑卒中55例(13.5%)、慢性阻塞性肺疾病急性加重54例(13.3%)、心衰急性发作52例(12.8%)、急性冠脉综合征38例(9.4%)、脓毒症35例(8.6%)、其他疾病18例(4.4%);12个月全因病死率为12.8%;住院时间为10 (6, 20) d。
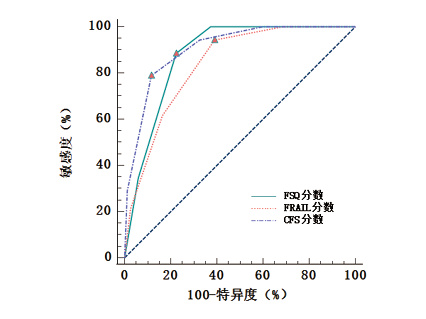
2.2 FSQ、FRAIL、CFS评分对12个月全因死亡预测效能的比较以12个月全因死亡为状态变量,FSQ、FRAIL、CFS评分为检测变量,绘制ROC曲线。见图 1。AUC(95%CI)依次为0.879(0.844~0.909)、0.838(0.798~0.872)、0.906(0.873~0.933)(均P < 0.001),CFS的AUC最大。以约登指数(youden index, YI)最大的点为界,FSQ、FRAIL、CFS评分预测12个月全因死亡的最佳截断值依次为3.0、2.0、7.0分。见表 1。
|
| 图 1 FSQ、FRAIL、CFS评分预测12个月全因死亡的ROC曲线 Fig 1 ROC curves of FSQ, FRAIL and CFS scores in predicting 12-month all-cause mortality |
|
|
| 变量 | AUC(95%CI) | 截断值 | YI | 敏感度 | 特异度 | Z值 | P值 |
| FSQ评分 | 0.879(0.844~0.909) | 3.0分 | 0.6615 | 0.8846 | 0.7768 | 22.849 | < 0.001 |
| FRAIL评分 | 0.838(0.798~0.872) | 2.0分 | 0.5525 | 0.9423 | 0.6102 | 14.764 | < 0.001 |
| CFS评分 | 0.906(0.873~0.933) | 7.0分 | 0.6726 | 0.7885 | 0.8842 | 22.442 | < 0.001 |
| 注:YI为约登指数,FSQ为衰弱筛查问卷,FRAIL为衰弱,CFS为临床衰弱量表 | |||||||
AUC两两比较结果提示,FSQ与CFS评分对12个月全因死亡的预测效能高于FRAIL评分(均P < 0.05),FSQ与CFS的预测效能差异无统计学意义(P > 0.05)。
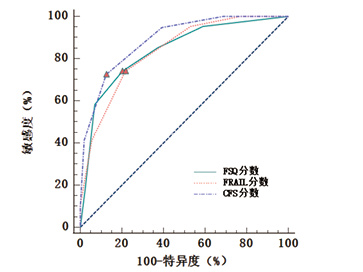
2.3 FSQ、FRAIL、CFS评分对12个月内失能预测效能的比较以12个月内是否发生失能(日常生活活动依赖)为状态变量,FSQ、FRAIL、CFS评分为检测变量,绘制ROC曲线。见图 2。AUC(95% CI)依次为0.840(0.801~0.874)、0.837(0.797~0.872)、0.889(0.854~0.918)(均P < 0.001),CFS的AUC最大。以YI最大的点为界,FSQ、FRAIL、CFS评分预测失能的最佳截断值依次为2.0、2.0、6.0分。见表 2。
|
| 图 2 FSQ、FRAIL、CFS评分预测12个月内失能的ROC曲线 Fig 2 ROC curves of FSQ, FRAIL and CFS scores in predicting dependence within 12 months |
|
|
| 变量 | AUC(95%CI) | 截断值 | YI | 敏感度 | 特异度 | Z值 | P值 |
| FSQ评分 | 0.840(0.801~0.874) | 2.0分 | 0.5380 | 0.7407 | 0.7972 | 17.379 | < 0.001 |
| FRAIL评分 | 0.837(0.797~0.872) | 2.0分 | 0.5242 | 0.7407 | 0.7834 | 18.223 | < 0.001 |
| CFS评分 | 0.889(0.854~0.918) | 6.0分 | 0.6004 | 0.7249 | 0.8756 | 26.276 | < 0.001 |
| 注:YI为约登指数,FSQ为衰弱筛查问卷,FRAIL为衰弱,CFS为临床衰弱量表 | |||||||
AUC两两比较结果示,CFS评分的预测效能高于FSQ、FRAIL评分(均P < 0.05);FSQ与FRAIL评分对12个月内失能的预测效能差异无统计学意义(P > 0.05)。
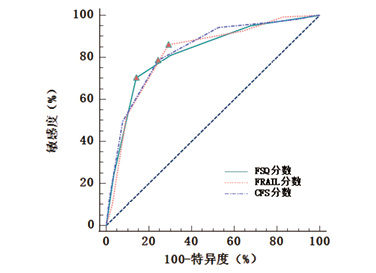
2.4 FSQ、FRAIL、CFS评分对12个月内再次发生急诊预测效能的比较以12个月内再次急诊就诊为状态变量,FSQ、FRAIL、CFS评分为检测变量,绘制ROC曲线。见图 3。AUC(95%CI)依次为0.821(0.780~0.857)、0.820(0.779~0.856)、0.830(0.790~0.865)(均P < 0.001),CFS的AUC最大。以YI最大的点为界,FSQ、FRAIL、CFS评分预测12个月内再次发生急诊的最佳截断值依次为3.0、2.0、6.0分。见表 3。
|
| 图 3 FSQ、FRAIL、CFS评分预测12个月内再次急诊的ROC曲线 Fig 3 ROC curves of FSQ, FRAIL and CFS scores in predicting re-admission to emergency |
|
|
| 变量 | AUC(95%CI) | 截断值 | YI | 敏感度 | 特异度 | Z值 | P值 |
| FSQ评分 | 0.821(0.780~0.857) | 3.0分 | 0.5621 | 0.7025 | 0.8596 | 13.950 | < 0.001 |
| FRAIL评分 | 0.820(0.779~0.856) | 2.0分 | 0.5683 | 0.8595 | 0.7088 | 14.412 | < 0.001 |
| CFS评分 | 0.830(0.790~0.865) | 6.0分 | 0.5430 | 0.7851 | 0.7579 | 15.183 | < 0.001 |
| 注:YI为约登指数,FSQ为衰弱筛查问卷,FRAIL为衰弱,CFS为临床衰弱量表 | |||||||
AUC两两比较结果示,FSQ、FRAIL、CFS评分对12个月内再次发生急诊预测效能的差异无统计学意义(均P > 0.05)。
2.5 急诊老年患者12个月生存分析共406例入选急诊老年患者完成随访,12个月全因死亡人数52例,病死率12.8%;以12个月全因死亡作为观察终点,进行生存分析。采用Cox比例风险回归模型分析衰弱与12个月死亡的相关性。
以FSQ评定衰弱与无衰弱,采用Log-rank检验进行生存比较,P < 0.001(χ2=16.151),见图 4A。调整性别、年龄、BMI、共患病后,FSQ衰弱是12个月全因死亡的独立危险因素(HRadj=3.267,95%CI: 2.406~4.435,P < 0.001)。见表 4。
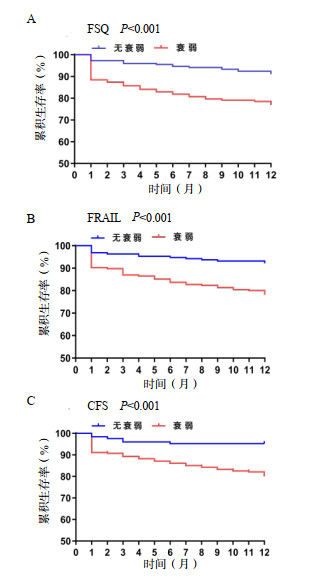
|
| 图 4 FSQ、FRAIL、CFS衰弱与无衰弱组12个月生存Kaplan-Meier曲线 Fig 4 Kaplan-Meier curves of 12-month survival in FSQ, FRAIL, CFS frail and non-frail groups |
|
|
| 影响因素 | B | S.E. | χ2 | df | P值 | HR | 95%CI |
| 性别 | |||||||
| 男性 | 0.000 | 1.000 | (基准组) | ||||
| 女性 | -0.322 | 0.300 | 1.152 | 1 | 0.283 | 0.725 | 0.402~1.305 |
| 年龄(岁) | 0.040 | 0.017 | 5.973 | 1 | 0.015 | 1.041 | 1.008~1.076 |
| BMI(kg/m2) | -0.129 | 0.037 | 12.461 | 1 | 0.001 | 0.879 | 0.818~0.944 |
| 共患病≥3个 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | 0.582 | 0.279 | 4.342 | 1 | 0.037 | 1.790 | 1.035~3.095 |
| 衰弱 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | 1.184 | 0.156 | 57.589 | 1 | < 0.001 | 3.267 | 2.406~4.435 |
| 注:FSQ为衰弱筛查问卷,BMI为身体质量质数 | |||||||
以FRAIL评定衰弱与无衰弱,采用Log-rank检验进行生存比较,P < 0.001(χ2=15.346),见图 4B。调整性别、年龄、BMI、共患病后,FRAIL衰弱是12个月全因死亡的独立危险因素(HRadj=2.465,95%CI: 1.819~3.341,P < 0.001)。见表 5。
| 影响因素 | B | S.E. | χ2 | df | P值 | HR | 95%CI |
| 性别 | |||||||
| 男性 | 0.000 | 1.000 | (基准组) | ||||
| 女性 | -0.465 | 0.293 | 2.524 | 1 | 0.112 | 0.628 | 0.354~1.115 |
| 年龄(岁) | 0.037 | 0.016 | 5.313 | 1 | 0.021 | 1.037 | 1.006~1.070 |
| BMI(kg/m2) | -0.053 | 0.035 | 2.348 | 1 | 0.125 | 0.948 | 0.886~1.015 |
| 共患病≥3个 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | -0.393 | 0.302 | 1.690 | 1 | 0.194 | 0.675 | 0.374~1.220 |
| 衰弱 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | 0.902 | 0.155 | 33.817 | 1 | < 0.001 | 2.465 | 1.819~3.341 |
| 注:BMI为身体质量质数 | |||||||
以CFS评定衰弱与无衰弱,采用Log-rank检验进行生存比较,P < 0.001(χ2=15.025),见图 4C。调整性别、年龄、BMI、共患病后,CFS衰弱是12个月全因死亡的独立危险因素(HRadj=3.523,95%CI: 2.648~4.687,P < 0.001)。见表 6。
| 影响因素 | B | S.E. | χ2 | df | P值 | HR | 95%CI |
| 性别 | |||||||
| 男性 | 0.000 | 1.000 | (基准组) | ||||
| 女性 | 0.108 | 0.338 | 0.102 | 1 | 0.749 | 1.114 | 0.575~2.159 |
| 年龄(岁) | 0.056 | 0.020 | 7.999 | 1 | 0.005 | 1.058 | 1.017~1.100 |
| BMI(kg/m2) | -0.112 | 0.036 | 9.604 | 1 | 0.002 | 0.894 | 0.833~0.960 |
| 共患病≥3个 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | 0.595 | 0.291 | 4.199 | 1 | 0.040 | 1.814 | 1.026~3.205 |
| 衰弱 | |||||||
| 否 | 0.000 | 1.000 | (基准组) | ||||
| 是 | 1.259 | 0.146 | 74.802 | 1 | < 0.001 | 3.523 | 2.648~4.687 |
| 注:CFS为临床衰弱量表,BMI为身体质量质数 | |||||||
为了应对人口老龄化的挑战,实现健康老龄化的目标,衰弱正成为世界范围内老年医学的研究热点[14-15]。目前,衰弱的评估量表有近70种,应用最广泛的两种衰弱评估工具为Fried衰弱表型(frailty phenotype, FP)[2]和Rockwood衰弱指数(Frailty index, FI)[16]。Fried FP首次实现了衰弱在临床实践的概念化,具有预测预后的价值;缺点是客观定量指标的测量较为耗时,并非所有老年人可完成。对繁忙的急诊科和急危重症患者,数据获得较为困难。FI为连续性数据,能更好地量化老年人的衰弱程度,个体FI越高,衰弱程度越重。FI对死亡等不良预后的预测价值较高,主要用于数据库回顾性分析及卫生经济分析等[9]。FI评估项目众多,多维度入选变量一般30~70个,评估过程耗时较长,需专业人员测评,并不适用于急诊科。此外,常用的衰弱筛查工具还有FRAIL[12]、CFS[13]、风险老年人识别(identification of seniors at risk, ISAR)[17]、维持自主综合服务研究计划7项问卷(programme on research for integrating services for the maintenance of autonomy 7 item questionnaire, PRISMA-7)等[18]。马丽娜等[9]基于Fried标准开发了自报告式衰弱筛查问卷FSQ,FSQ不过多依赖客观指标,评估简单快速,对临床结局的预测通过北京老龄化多维纵向调查[19]、中国健康与养老追踪调查[20]等大型队列研究验证,本团队的研究[21]验证了FSQ预测急诊老年患者短期预后的有效性。
Lewis等[10] 2019年的多中心前瞻性队列研究采用稳定、不稳定、帮助行走、卧床(stable, unstable, help to walk, bedbound, SUHB)量表、FP、CFS 3种工具评估衰弱,于出院后3~6个月内进行随访,终点事件包括死亡、自评生活质量或健康状况差、需要社区服务、再次急诊就诊。结果显示衰弱与3~6个月不良预后呈正相关,SUHB、FP、CFS评分预测预后的AUC分别为0.720、0.735、0.730,CFS使用简单、限制因素少、耗时短,是急诊科实用的衰弱评估量表。Fehlmann等[22]综述了CFS量表在急诊科的应用,34项研究纳入最终分析,研究多应用CFS作为主要暴露、潜在预测因子,最常用终点是病死率和住院率,可见CFS在急诊医学研究中的应用正在急剧增加。O'Caoimh等[11]在急诊科70岁以上患者中进行CFS、ISAR、PRISMA-7评分,采用综合老年评估诊断衰弱,3种量表的AUC依次为0.83、0.78、0.88,PRISMA-7区分衰弱与无衰弱的准确性高于ISAR,与CFS差异无统计学意义。
本研究在急诊科60岁及以上的患者中进行FSQ、FRAIL、CFS量表评分,随访12个月,以全因死亡、失能、再次发生急诊为终点事件,3种量表预测终点事件的AUC范围为0.820~0.906,除12个月内再次发生急诊这一结局的预测效能三者差异无统计学意义外,CFS对其他终点事件的预测准确性高于另外一种或者两种量表;与既往研究一致。本研究还发现3种量表筛查的衰弱均与12个月全因死亡独立相关(HR范围为2.465~3.523)。但数据来源于单一临床中心,排除急诊留观时间 < 24 h及需急诊手术患者,存在选择偏倚,样本量较小,为本研究的局限性;结论的可重复性仍需多中心大样本研究验证。
我国老年人口数量和老龄化速度均居世界首位,衰弱与老年人负性临床结局密切相关。衰弱的快速评估有助于为患者出院后需要怎样的支持措施提供预警。在急诊科筛查衰弱是为了防止不必要的检查或治疗对衰弱的老年人造成伤害;健壮和衰弱前期的老年人也将受益于量身定制的训练与护理计划,以恢复某些功能,减缓衰弱进程。因此急诊老年患者应尽早识别衰弱。CFS量表简单快捷,是适用于急诊科衰弱筛查的有效工具,但有一定的主观性,需规范应用。
利益冲突 所有作者声明无利益冲突
作者贡献声明 刘慧珍:实施研究、文章撰写;王国栋:获取研究经费、支持性贡献;商永、李俊玉、刘小蒙:数据收集及整理;商娜:统计学分析;王娜:行政支持;郭树彬:实验设计、研究指导;马素霞:对文章内容做批评性审阅、文章修改
| [1] | Beard JR, Officer A, de Carvalho IA, et al. The world report on ageing and health: a policy framework for healthy ageing[J]. Lancet, 2016, 387(10033): 2145-2154. DOI:10.1016/S0140-6736(15)00516-4 |
| [2] | Fried LP, Tangen CM, Walston J, et al. Frailty in older adults: evidence for a phenotype[J]. J Gerontol A Biol Sci Med Sci, 2001, 56(3): M146-M156. DOI:10.1093/gerona/56.3.m146 |
| [3] | Clegg A, Young JB, Iliffe S, et al. Frailty in elderly people[J]. Lancet, 2013, 381: 752-762. DOI:10.1016/S0140-6736(12)62167-9 |
| [4] | 中华医学会老年医学分会, 《中华老年医学杂志》编辑委员会. 老年人衰弱预防中国专家共识(2022)[J]. 中华老年医学杂志, 2022, 41(5): 503-511. DOI:10.3760/cma.j.issn.0254-9026.2022.05.001 |
| [5] | 刘金炜, 王芳, 张倪惠, 等. 卧床患者衰弱的运动干预[J]. 中华老年医学杂志, 2022, 41(4): 483-487. DOI:10.3760/cma.j.issn.0254-9026.2022.04.024 |
| [6] | Zhang XM, Cao SM, Gao MF, et al. The prevalence of social frailty among older adults: a systematic review and meta-analysis[J]. J Am Med Dir Assoc, 2023, 24(1) 29-37. e9. DOI:10.1016/j.jamda.2022.10.007 |
| [7] | Zhou Q, Li Y, Gao Q, et al. Prevalence of frailty among Chinese community-dwelling older adults: a systematic review and meta-analysis[J]. Int J Public Health, 2023, 68: 1605964. DOI:10.3389/ijph.2023.1605964 |
| [8] | 商娜, 郭树彬. 衰弱评估: 老年急诊领域的机遇和挑战[J]. 中国急救医学, 2022, 42(6): 541-544. DOI:10.3969/j.issn.1002-1949.2022.06.015 |
| [9] | 马丽娜, 陈彪. 老年人衰弱综合征的研究现状及发展趋势[J]. 中华老年医学杂志, 2020, 39(4): 369-372. DOI:10.3760/cma.j.issn.0254-9026.2020.04.001 |
| [10] | Lewis ET, Dent E, Alkhouri H, et al. Which frailty scale for patients admitted via emergency department? A cohort study[J]. Arch Gerontol Geriatr, 2019, 80: 104-114. DOI:10.1016/j.archger.2018.11.002 |
| [11] | O'Caoimh R, Costello M, Small C, et al. Comparison of frailty screening instruments in the emergency department[J]. Int J Environ Res Public Health, 2019, 16(19): 3626. DOI:10.3390/ijerph16193626 |
| [12] | Morley JE, Malmstrom TK, Miller DK. A simple frailty questionnaire (FRAIL) predicts outcomes in middle aged African Americans[J]. J Nutr Health Aging, 2012, 16(7): 601-608. DOI:10.1007/s12603-012-0084-2 |
| [13] | Rockwood K, Song XW, MacKnight C, et al. A global clinical measure of fitness and frailty in elderly people[J]. CMAJ, 2005, 173(5): 489-495. DOI:10.1503/cmaj.050051 |
| [14] | Gwyther H, Shaw R, Jaime Dauden EA, et al. Understanding frailty: a qualitative study of European healthcare policy-makers' approaches to frailty screening and management[J]. BMJ Open, 2018, 8(1): e018653. DOI:10.1136/bmjopen-2017-018653 |
| [15] | Buckinx F, Rolland Y, Reginster JY, et al. Burden of frailty in the elderly population: perspectives for a public health challenge[J]. Arch Public Health, 2015, 73(1): 19. DOI:10.1186/s13690-015-0068-x |
| [16] | Mitnitski AB, Mogilner AJ, Rockwood K. Accumulation of deficits as a proxy measure of aging[J]. Sci World J, 2001, 1: 323-336. DOI:10.1100/tsw.2001.58 |
| [17] | Elliott A, Phelps K, Regen E, et al. Identifying frailty in the emergency department-feasibility study[J]. Age Ageing, 2017, 46(5): 840-845. DOI:10.1093/ageing/afx089 |
| [18] | Dent E, Kowal P, Hoogendijk EO. Frailty measurement in research and clinical practice: a review[J]. Eur J Intern Med, 2016, 31: 3-10. DOI:10.1016/j.ejim.2016.03.007 |
| [19] | Ma L, Tang Z, Chan P, et al. Novel frailty screening questionnaire (FSQ) predicts 8-year mortality in older adults in China[J]. J Frailty Aging, 2019, 8(1): 33-38. DOI:10.14283/jfa.2018.38 |
| [20] | Wu CK, Smit E, Xue QL, et al. Prevalence and correlates of frailty among community-dwelling Chinese older adults: the China health and retirement longitudinal study[J]. J Gerontol A Biol Sci Med Sci, 2017, 73(1): 102-108. DOI:10.1093/gerona/glx098 |
| [21] | Liu H, Shang N, Chhetri JK, et al. A frailty screening questionnaire (FSQ) to rapidly predict negative health outcomes of older adults in emergency care settings[J]. J Nutr Health Aging, 2020, 24(6): 627-633. DOI:10.1007/s12603-020-1374-8 |
| [22] | Fehlmann CA, Nickel CH, Cino E, et al. Frailty assessment in emergency medicine using the clinical frailty scale: a scoping review[J]. Intern Emerg Med, 2022, 17(8): 2407-2418. DOI:10.1007/s11739-022-03042-5 |
 2025, Vol. 34
2025, Vol. 34